
 El objetivo de esta charla es cómo descargar cognitivamente nuestra mente mientras realizamos una reanimación. ACLS nos proporciona un marco para el tratamiento de víctimas adultas de paro cardíaco (CA) u otras emergencias cardiopulmonares. Esto ayuda a que los proveedores que normalmente no se ocupan de la AC mejoren cosas, como la calidad de la RCP, minimizando las interrupciones durante la RCP para controlar el pulso y el momento/dosificación de la epinefrina. La Medicina de Emergencia (ME) y el mundo prehospitalario son diferentes a muchos entornos de la medicina. Recibimos una información mínima en el momento de la llegada del paciente y al mismo tiempo el proceso de la enfermedad que está teniendo lugar no se ha definido del todo. Se espera constantemente de nosotros que manejemos y resucitemos de manera precisa a cualquiera que entre a nuestras puertas las 24 horas del día, los 7 días de la semana, los 365 días del año, muchas veces sin información crucial. Por lo tanto, nuestro trabajo debería ser garantizar que la perfusión coronaria y cerebral sea de la más alta calidad, pero también, al mismo tiempo, juntar las piezas del rompecabezas para descubrir por qué nuestro paciente está en CA. Puede resultar muy difícil hacer ambas cosas y muchas veces sacrificamos una por la otra. Por lo tanto, es importante descargarnos cognitivamente durante la reanimación de nuestros pacientes en CA y centrar nuestra atención en por qué están en CA. Como revelación para esta conferencia, dije que algunas de las recomendaciones hechas tienen evidencia que las respalda y otras son más teóricas y ciertamente están sujetas a discusión.
El objetivo de esta charla es cómo descargar cognitivamente nuestra mente mientras realizamos una reanimación. ACLS nos proporciona un marco para el tratamiento de víctimas adultas de paro cardíaco (CA) u otras emergencias cardiopulmonares. Esto ayuda a que los proveedores que normalmente no se ocupan de la AC mejoren cosas, como la calidad de la RCP, minimizando las interrupciones durante la RCP para controlar el pulso y el momento/dosificación de la epinefrina. La Medicina de Emergencia (ME) y el mundo prehospitalario son diferentes a muchos entornos de la medicina. Recibimos una información mínima en el momento de la llegada del paciente y al mismo tiempo el proceso de la enfermedad que está teniendo lugar no se ha definido del todo. Se espera constantemente de nosotros que manejemos y resucitemos de manera precisa a cualquiera que entre a nuestras puertas las 24 horas del día, los 7 días de la semana, los 365 días del año, muchas veces sin información crucial. Por lo tanto, nuestro trabajo debería ser garantizar que la perfusión coronaria y cerebral sea de la más alta calidad, pero también, al mismo tiempo, juntar las piezas del rompecabezas para descubrir por qué nuestro paciente está en CA. Puede resultar muy difícil hacer ambas cosas y muchas veces sacrificamos una por la otra. Por lo tanto, es importante descargarnos cognitivamente durante la reanimación de nuestros pacientes en CA y centrar nuestra atención en por qué están en CA. Como revelación para esta conferencia, dije que algunas de las recomendaciones hechas tienen evidencia que las respalda y otras son más teóricas y ciertamente están sujetas a discusión.
También asegúrese de visitar nuestro canal de YouTube.

Esta publicación también se publica en el blog de St. Emlyn: Más allá de A(C)LS
Comencemos con un caso:
Un hombre caucásico de 64 años ha presenciado un paro cardíaco fuera del hospital (OHCA). Se desconoce su historial médico. Recibe RCP iniciada por un transeúnte, lo intuban prehospitalariamente mediante servicios de emergencias médicas y lo llevan al servicio de urgencias sin pulso, el último ritmo fue PEA y el acceso intravenoso se perdió en el camino.
El resto de esta publicación se centrará en ir más allá del ACLS y la descarga cognitiva durante el arresto en lo que respecta a:
- RCP
- Acceso
- Vías respiratorias
- Epinefrina
- Evaluación de PEA
- Comprobaciones de pulso
Reanimación cardiopulmonar (RCP)
La Asociación Estadounidense del Corazón y el Colegio Estadounidense de Cardiología (AHA/ACC) de 2015 publicaron una nueva actualización sobre la calidad de la RCP en circulación [1]. Los puntos clave del resumen fueron:
- Frecuencia: 100 – 120 compresiones/min
- Profundidad: 2 – 2,4 pulgadas
- Retroceso: Permitir retroceso total
- Interrupciones: Minimiza las Pausas
Un artículo de revisión de Cunningham LM et al [2] demostró que incluso pausas breves en la RCP pueden provocar una disminución de la presión de perfusión coronaria (consulte la figura siguiente). La presión de perfusión disminuida no vuelve inmediatamente a niveles adecuados al reiniciar la RCP. La disminución de la presión de perfusión coronaria en realidad dura más que la pausa en sí y lleva tiempo aumentar gradualmente la presión hasta un nivel inicial, lo que significa que el tejido cardíaco en realidad es isquémico y no está perfundido durante un período más largo que la pausa en sí. Esto es importante porque es menos probable que el tejido cardíaco isquémico se desfibrile con éxito en ritmos desfibrilables.
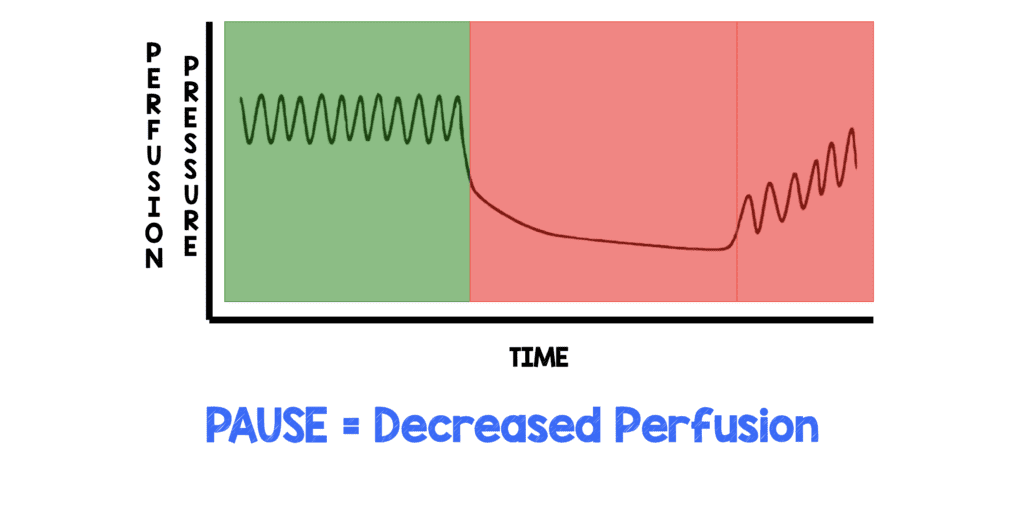
Se necesita bastante ancho de banda mental para garantizar que la RCP se realice bien y que ya haya suficiente actividad durante la reanimación, entonces, ¿hay alguna manera de que podamos descargar cognitivamente nuestras mentes?
Gates S et al realizaron una revisión sistemática y un metanálisis de ensayos clínicos aleatorios que intentaron responder a la pregunta sobre RCP mecánica versus RCP manual en OHCA por Gates S et al en Resuscitation 2015 [3]. El ensayo incluyó cinco ensayos clínicos aleatorios (ECA) con más de 10.000 pacientes con OHCA. Al final, el estudio no encontró diferencias en ROSC, supervivencia o supervivencia con buenos resultados neurológicos. Ninguno de los estudios mostró superioridad de la RCP mecánica, pero tampoco ninguno de los estudios mostró inferioridad a la RCP manual. En otras palabras, la RCP mecánica hasta la fecha no es ni mejor ni peor que la RCP manual.
Conclusión clínica: realizar una RCP ininterrumpida de alta calidad es importante, pero este no es el criterio de valoración de la reanimación. La RCP mecánica es una excelente manera de descargar nuestras mentes. Ahora no tenemos que centrarnos en la frecuencia de las compresiones, la profundidad de las compresiones, las interrupciones de las compresiones y, en cambio, centrarnos en por qué nuestro paciente ha tenido una AC.
Nuestro paciente: A nuestro paciente se le inicia RCP mecánica, pero recuerde que EMS perdió el acceso intravenoso...
Acceso
Recientemente pregunté en Twitter, en un paciente con CA y sin acceso intravenoso, ¿cuál es su acceso? Los resultados están a continuación:
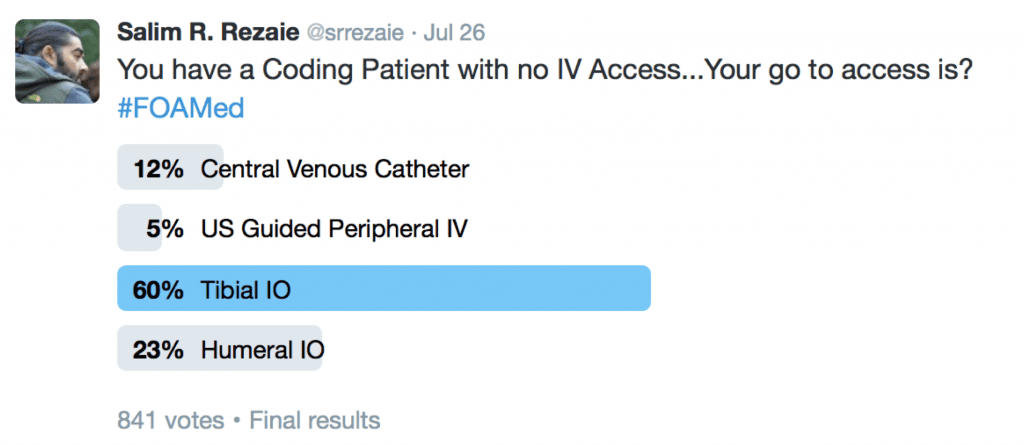
En mi opinión, en realidad solo hay dos sitios para el acceso intraóseo (IO) durante la CA: la cabeza humeral o la tibia proximal. Se ha demostrado que la IO esternal proporciona una velocidad de infusión más rápida que otros sitios, pero puede obstaculizar la RCP en la CA [10]. El húmero proximal está más cerca del corazón y, por lo tanto, hace que los medicamentos circulen más rápido que la tibia proximal. Por otro lado, la tibia proximal está alejada de la cabecera de la cama, que es donde normalmente se reúne la mayoría de las personas para el manejo de las vías respiratorias y la RCP. Otra forma de pensar en los sitios de acceso IO son:
- Cabeza humeral y IO esternal = Catéter venoso central (más cerca del corazón)
- Tibial IO = Acceso intravenoso periférico (más distal al corazón)
Hubo un ECA realizado por Reades et al en Ann Emerg Med 2011 [4], que es el ECA más grande hasta la fecha que compara IO humeral versus IO tibial versus IV periférica (PIV). Este estudio incluyó a 183 pacientes con OHCA. Su resultado primario fue el éxito del primer intento de acceso y un resultado secundario fue el tiempo de acceso.
-
Primer intento exitoso:
- Tibia IO: 91%
- IO humeral: 51%
- PIV: 43%
-
Tiempo de acceso (min)
- IO tibial: 4,6
- IO humeral: 7,0
- PIV: 5,8
- Una gran advertencia para este ensayo es que se trató de un estudio prehospitalario y no de un estudio en el servicio de urgencias. En segundo lugar, puede haber habido algún problema con la familiaridad con la colocación de las OI humerales, como lo demuestra el tiempo de acceso (¿7 minutos?!?).
Conclusión clínica: cuando se tiene dificultad para obtener un acceso intravenoso durante la CA, la IO humeral tiene una mayor tasa de éxito y un tiempo de acceso más rápido que la intravenosa.
Nuestro paciente: Recibe dos IO de húmero proximal de calibre 15 y varias personas comienzan a preguntar sobre el manejo de las vías respiratorias.
Vías respiratorias
VÍAS AÉREAS-2 [11]
Qué hicieron: Este fue un ensayo clínico multicéntrico, aleatorizado por grupos, de paramédicos de cuatro servicios de ambulancia en Inglaterra. El objetivo del estudio fue determinar si un dispositivo supraglótico para la vía aérea (SGA) es superior a la intubación traqueal (IT) como estrategia inicial avanzada de manejo de la vía aérea en adultos con OHCA no traumática.
- *Curiosamente, aleatorizar a los pacientes en el momento de la OHCA se consideró poco práctico; por lo tanto, los paramédicos fueron aleatorizados para utilizar 1 de 2 estrategias avanzadas de manejo de las vías respiratorias para los pacientes elegibles que trataron.
- SGA = Dispositivo de vía aérea supraglótica de segunda generación con un manguito suave no inflable (i-gel; interquirúrgico)
- TI = Laringoscopia directa como videolaringoscopia no utilizada por los paramédicos en Inglaterra.
- 9.296 pacientes inscritos en el ensayo
- Grupo SGA = 4886
- Grupo TI = 4410
- Buena puntuación mRS (0 – 3) en Hospital DC o 30 días:
- EGA = 6,4%
- TI = 6,8%
- RD ajustada -0,6%; IC del 95 %: -1,6 % – 0,4 %
- 1.707 de los pacientes no recibieron ningún tratamiento avanzado de las vías respiratorias
- Supervivencia con buenos resultados neurológicos
- TI pero sin manejo avanzado de las vías respiratorias = 21,6 %
- PEG pero sin manejo avanzado de las vías respiratorias = 20,5%
- Supervivencia con buenos resultados neurológicos
- El uso del manejo avanzado de las vías respiratorias fue mayor entre los paramédicos del grupo de dispositivos supraglóticos de vías respiratorias (85%) en comparación con los del grupo de intubación traqueal (78%), lo que también podría generar confusión según la indicación.
- El uso de dispositivos de vía aérea supraglótica como la primera técnica avanzada de vía aérea en OHCA se asoció con mejores resultados; sin embargo, las diferencias entre los grupos fueron menores que la diferencia clínicamente importante preespecificada y menores que la diferencia mínimamente importante de ≈3% informada en otros estudios. .Por lo tanto, esta es una hipótesis que genera una conclusión.
- Un artículo de Jabre P et al [12] que compara BVM versus TI para el manejo de las vías respiratorias durante la OHCA en >2000 pacientes en Francia y Bélgica. El resultado primario fue el resultado neurológico favorable a los 28 días. Básicamente no hubo diferencias en este resultado entre los grupos (4,3 % frente a 4,2 %; IC del 95 %: -7,7 % – 0,3 %).
- Conclusión clínica: entre los pacientes con OHCA, parece que la clave para el manejo de las vías respiratorias parece ser elegir una estrategia que no interfiera con las cosas más importantes para lograr una mejor supervivencia con buenos resultados neurológicos (es decir, RCP de alta calidad). .
Nuestro paciente: Recibe una vía aérea supraglótica (SGA y ahora varias personas en la sala comienzan a pedir epinefrina (adrenalina)
Dosificación/momento de la epinefrina
Lo que el twitterverse siente es la dosis y el momento correctos de la epinefrina en CA:
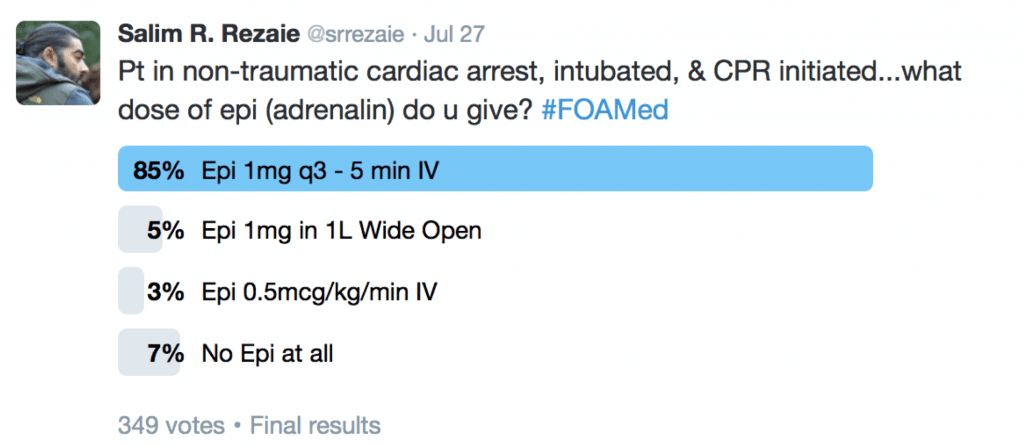
Las pautas de soporte vital cardíaco avanzado (ACLS) para adultos de 2015 recomiendan que QUIZÁS sea razonable administrar epinefrina 1 mg por vía intravenosa cada 3 – 5 minutos, tal vez sea razonable [5]. Le dan a esto una recomendación de Clase IIb, que es otra forma de decir evidencia débil (Beneficio ≥ Riesgo).
Muchos estudios que analizan los resultados con la dosificación de epinefrina recomendada por ACLS analizan resultados sustitutos, específicamente ROSC. En CA, ROSC es el primer paso, pero lo que realmente nos importa es la supervivencia neurológicamente intacta. Hasta la fecha, no existe ningún estudio que haya demostrado que la epinefrina en la CA mejore la supervivencia neurológicamente intacta.
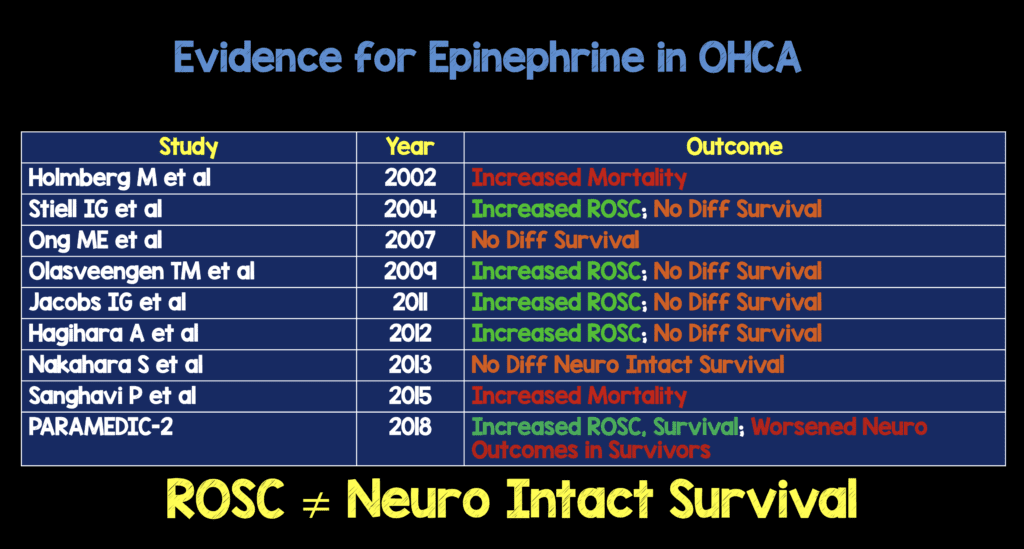
La epinefrina produce algunos efectos beneficiosos en la CA de aumento de la presión de perfusión coronaria y de la presión de perfusión cerebral durante la RCP, pero en dosis en bolo puede aumentar el consumo de oxígeno del miocardio y, por lo tanto, aumentar la isquemia subendocárdica.
PARAMÉDICO-2 [13]
Qué hicieron: Evaluación prehospitalaria del papel de la adrenalina: medición de la eficacia de la administración de fármacos en el paro cardíaco (PARAMEDIC-2). Se trata de un ensayo multicéntrico, aleatorizado, doble ciego y controlado con placebo en el que participaron 8.014 pacientes con OHCA en el Reino Unido.
- 8014 pacientes con OHCA
- 4015 en el grupo de epinefrina intravenosa (Epi)
- 3999 en el grupo de placebo de solución salina intravenosa (Placebo)
- Supervivencia al Hospital DC con resultado neurológico favorable
- Epi: 2,2%
- Placebo: 1,9%
- uOR 1.1
- Deterioro neurológico severo (mRs 4 – 5)
- Epi 31,0%
- Placebo 17,8%
- Punto clínico para recordar: En este ensayo multicéntrico bien realizado, la epinefrina administrada a 1 mg cada 3 – 5 minutos aumentó las posibilidades de ROSC, pero tuvo el costo de un mayor uso de la UCI, más pacientes con discapacidades neurológicas graves y ninguna diferencia en la supervivencia con condiciones neurológicas favorables. resultado en comparación con placebo . El uso de 1 mg de epinefrina cada 3 a 5 minutos ya no debería formar parte de los protocolos estándar de paro cardíaco. La epinefrina debe ser administrada caso por caso por proveedores experimentados que perciban que se puede obtener un beneficio.
Ahora seré el primero en admitir que puede causar un malestar excesivo en la dinámica de su equipo durante la reanimación si recomienda omitir la epinefrina por completo sin una explicación muy extensa. En cambio, tengo otras dos opciones a considerar que eliminarán la distracción de recordar la epinefrina cada 3 a 5 minutos:
- Opción 1: The Dirty Epi Drip : introduzca 1 mg (es decir, 1 ampolla) de epinefrina del carrito de código en 1000 ml de NS, lo que le dará una concentración final de 1 mcg/ml. Puede abrirlo completamente con una bolsa de presión hasta que, a) la hemodinámica de su paciente se estabilice, ob) un goteo de epinefrina esté listo para su uso.
- Opción 2: Epi Drip de un cuarto de dosis: ejecute epinefrina a 0,5 mcg/kg/min. En un paciente de 100 kg, esto equivaldría a 250 mcg durante 5 minutos (es decir, un cuarto de dosis).
Ejecutar un goteo de epinefrina permite que ocurran varias cosas:
- Descarga cognitiva: nadie tiene que recordar "es hora del próximo episodio", cada 3 a 5 minutos
- Minimizar la labilidad fisiológica: la dosis continua de epinefrina permite una presión de perfusión coronaria y cerebral más suave sin aumentar el consumo de oxígeno del miocardio ni isquemia subendocárdica (ésta es mi opinión, pero no hay estudios que comparen el goteo epi con la dosis estándar de 1 mg de epi cada 3 – 5 minutos en CA)
- Evitar la caída de la presión arterial posterior al ROSC: ajustar el goteo a la dosis necesaria
Conclusión clínica: Ningún estudio hasta la fecha ha demostrado que la ACLS recomendó 1 mg de epinefrina cada 3 – 5 minutos mejore la supervivencia neurológicamente intacta en la CA. Quizás una mejor manera sería realizar una infusión continua de epinefrina en dosis más bajas.
Nuestro paciente: comienza con un goteo de Epi sucio y se pasa a un goteo de Epi de un cuarto de dosis.
Evaluación de PEA
Aproximadamente 1/3 de los pacientes en CA tienen PEA y es bien sabido que los pacientes con PEA como ritmo inicial tienen una peor supervivencia que los pacientes con un ritmo desfibrilable [6]. Si eres como yo, habrás aprendido todo sobre las H y T que potencialmente podrían causar PEA, pero incluso ahora intenta enumerarlas todas. Ahora imagínese tratando de superar este diferencial mientras resucita a un paciente en PEA CA. Pittman et al publicaron un interesante artículo en Med Princ Pract 2014 [6] que se centró en las pocas causas de PEA que podemos corregir rápida y eficazmente en lugar de memorizar las tradicionales H y T. Los pasos de su algoritmo son simples:
- Determinar si la PEA es estrecha (Duración QRS <0,12) o ancha (Duración QRS ≥0,12)
- La PEA de complejo estrecho generalmente se debe a problemas mecánicos causados por la obstrucción del flujo de entrada o salida del ventrículo derecho.
- La PEA de complejo ancho generalmente se debe a problemas metabólicos.

- Un estudio posterior [14] demostró que el ancho del QRS no predecía la causa de la PEA. En el estudio de seguimiento se observaron prospectivamente 51 pacientes con parada por IHCA y PEA. La conclusión fue que no había patrones únicos de ECG asociados con la causa subyacente de la PEA (considere esta teoría desacreditada).
-
El examen CASA [15]
- Qué hicieron: descripción de un algoritmo POCUS simplificado durante un paro cardíaco. El examen consta de tres exámenes POCUS de <10 segundos durante las comprobaciones de ritmo, como se muestra en la imagen a continuación. La visión óptima sugerida es una sonda de matriz en fase utilizada en la vista subxifoidea, ya que esta vista no interrumpe la RCP. Un punto clave es que alguien cuente en voz alta para no prolongar las pausas de la RCP y que registre durante la ecografía para poder revisar las imágenes después de reanudar la RCP. Finalmente, E-FAST se puede realizar caso por caso según los autores.
- Paso 1: Según los autores, el derrame pericárdico que causa taponamiento cardíaco es la causa del paro cardíaco en entre el 4 y el 15% de los pacientes. El taponamiento se puede intervenir con el uso de pericardiocentesis.
- Paso 2: Los autores afirman que la embolia pulmonar es la causa del paro cardíaco en entre el 4,0 y el 7,6% de los pacientes. La evidencia de tensión del corazón derecho debería colocar a la embolia pulmonar en un lugar más alto en el diferencial, pero puede haber otras causas de tensión del corazón derecho. Si se diagnostica EP, se recomienda la trombólisis sistémica.
- Paso 3: Finalmente, los autores afirman que la presencia o ausencia de actividad cardíaca puede proporcionar información pronóstica útil. Obviamente, la ausencia de actividad cardíaca en la PEA presagia peores resultados (tasa de supervivencia hasta el alta hospitalaria = 0,0% – 0,6%). Este hallazgo, junto con otros factores de mal pronóstico, como el bajo nivel de CO2 al final de la espiración, el tiempo de inactividad prolongado y el paro no presenciado, pueden ayudar en la utilidad de la reanimación continua.
- Pasos auxiliares: el neumotórax a tensión es una causa rara de paro cardíaco no traumático, pero puede evaluarse por la ausencia de deslizamiento pulmonar en POCUS en la parte anterior del tórax. Si se detecta, se puede considerar la descompresión con aguja o la toracostomía con el dedo o con tubo.
- Punto clínico para recordar: POCUS se ha convertido en una de las herramientas más importantes para descubrir tanto el diagnóstico como el tratamiento de pacientes críticamente enfermos. Sin embargo, la literatura más reciente indica que el uso de POCUS prolonga las pausas de la RCP, lo que en última instancia afecta la buena supervivencia neurológica. Los protocolos POCUS, como el examen CASA, pueden ayudar a disminuir la carga cognitiva y minimizar las pausas.

Nuestro paciente: Nuestro paciente se somete al examen CASA y la ecografía a pie de cama encuentra un VD > VI dilatado y preocupación por una EP masiva. El paciente recibe tPA sistémico y presenta un cambio de ritmo en el monitor. Alguien grita, ¿puedes sentir el pulso?
Comprobaciones de pulso
¿Cuál cree el twitterverse que es la mejor manera de verificar el ROSC en CA? Los resultados están a continuación:
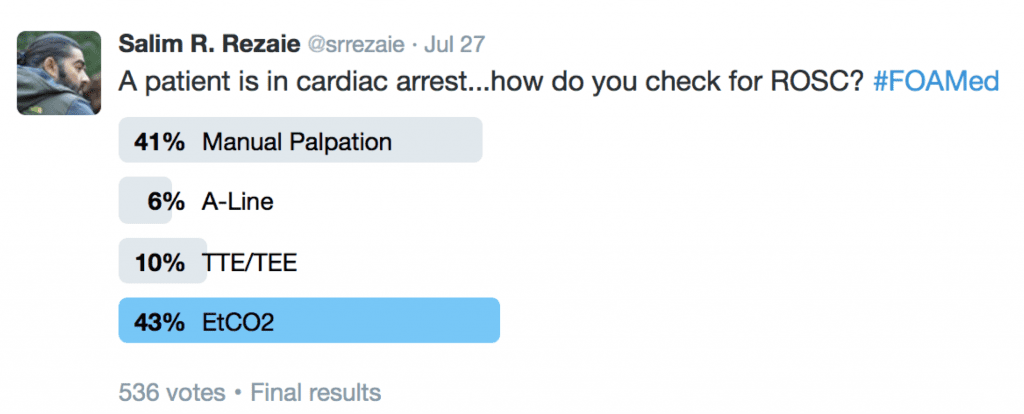
Ochoa FJ et al publicaron un ensayo en Resuscitation 1998 [7] en el que médicos del servicio de urgencias, médicos de la UCI y enfermeras intentaron identificar el pulso carotídeo en un voluntario varón sano con presión arterial normal. El 43,1% de los profesionales de la salud requirió >5 segundos para detectar el pulso carotídeo y el 4,3% requirió >10 segundos.
Entonces, ¿la verificación manual del pulso está muerta? Tal vez. Ciertamente creo que tenemos mejores tecnologías para ayudar a determinar el ROSC que no requieren pausas en la RCP:
- Línea arterial: el beneficio de la línea arterial es que obtenemos información directa sobre el gasto cardíaco, pero la desventaja es que lleva tiempo colocarla.
- Ecocardiograma transtorácico (ETT) junto a la cama: esto le brinda al proveedor información en tiempo real de lo que el corazón está haciendo en realidad (es decir, no sentir el pulso manualmente, cuando en realidad el corazón se está contrayendo débilmente - Pseudo PEA), también puede brindar información en tiempo real sobre la calidad de la RCP. y potencialmente tiene la capacidad de predecir las posibilidades de ROSC [8]. La desventaja es que todavía tenemos que detener la RCP para buscar actividad cardíaca, pero si se hace correctamente no debería tomar más de 10 segundos para ver si el VI se está contrayendo o no. Blyth L publicó una revisión sistemática de pacientes en CA en Academic Emergency Medicine 2012 [8]. Esto incluyó 8 estudios con 568 pacientes con OHCA a quienes se les realizó un ecocardiograma a pie de cama. A los 20 minutos, si había movimiento cardíaco en la ecografía, el 51,6% de los pacientes logró un ROSC y el 48,4% no logró un ROSC. Por otro lado, si no había movimiento cardíaco a los 20 minutos en la ecografía a pie de cama, sólo el 2,4% logró un ROSC, mientras que el 97,6% no. Un problema importante de este estudio es que se utilizó ROSC como marcador sustituto y no se evaluaron los resultados neurológicos.
-
Fin del CO2 mareal (EtCO2): Para mí, aquí es donde está el dinero. Ahrens T et al analizaron el EtCO2 en OHCA como un indicador pronóstico de los resultados [9] y descubrieron que un EtCO2 <10 – 15 mmHg a los 20 minutos predecía una probabilidad de supervivencia del 0,8%. Los estudios que evalúan el uso de EtCO2 en AC han sido en pacientes intubados, estudios observacionales y hasta la fecha ninguno ha investigado la supervivencia con resultado neurológico intacto. Las directrices de la AHA/ACC de 2015 en realidad establecen que en pacientes intubados, la imposibilidad de alcanzar un EtCO2 de >10 mmHg mediante capnografía de forma de onda después de 20 minutos de RCP puede considerarse como un componente de un enfoque multimodal para decidir cuándo finalizar los esfuerzos de reanimación, pero no debe considerarse utilizado de forma aislada (ClaseIIb)[5]. Actualmente no existe una duración óptima de la reanimación antes de la finalización de la reanimación (TOR).
- Los pulmones requieren ventilación y perfusión para funcionar. Si mantenemos la ventilación constante con una máscara de válvula de bolsa o un ventilador, entonces la perfusión es el único factor que no se tiene en cuenta. Por lo tanto, un aumento en el gasto cardíaco debería aumentar la lectura de EtCO2. Sin embargo, cualquier cosa que interrumpa la ventilación provocará lecturas falsas de EtCO2 (es decir, tubo endotraqueal desalojado, causas respiratorias de CA y embolia pulmonar).
Conclusión clínica: Detener la RCP para controlar el pulso no es exacto para predecir el ROSC y es potencialmente perjudicial para los resultados neurológicos de los pacientes. Los complementos como la ecocardiografía a pie de cama y el EtCO2 se suman a un enfoque multimodal para predecir el ROSC y brindan información útil en las decisiones de finalización de la reanimación.
Nuestro paciente: Se le colocó EtCO2 y después de los trombolíticos tuvo un salto en su EtCO2 a 30 mmHg y se encontró que tenía ROSC en la ecografía junto a la cama.
Puntos críticos para ir más allá del ACLS y descargar cognitivamente durante los esfuerzos de reanimación de un paro cardíaco:
- RCP: RCP mecánica > RCP manual
- Acceso: Acceso IO > Acceso IV
- Vía aérea: SGA > BVM > ETI
- Epinefrina: Goteo de epinefrina > Bolo de epinefrina
- Evaluación de PEA: POCUS (examen CASA) > H y T
- Controles de pulso: EtCO2 + TTE de cabecera > Controles de pulso manuales
Para obtener más información sobre este pago:
- Jonathan St. George en The Ember Project: El dispositivo Lucas y la descarga cognitiva
- Anton Helman en EM Cases: Episodio 96 – Más allá del paro cardíaco ACLS – En vivo desde la Conferencia EMU 2017
Referencias:
- Kleinman ME et al. Calidad de la reanimación cardiopulmonar y soporte vital básico para adultos: Actualización de las directrices de la Asociación Estadounidense del Corazón de 2015 para reanimación cardiopulmonar y atención cardiovascular de emergencia. Circulación 2015; 132 (18 Suplemento 2): S414 – 25. PMID: 264722993
- Cunningham LM et al. Reanimación cardiopulmonar en caso de paro cardíaco: la importancia de las compresiones torácicas ininterrumpidas en la reanimación de un paro cardíaco. Am J Emerg Med 2012; 30(8): 1630 – 8. PMID: 22633716
- Gates S et al. Compresión torácica mecánica para paro cardíaco extrahospitalario: revisión sistemática y metanálisis. Reanimación 2015; 94: 91 – 7. PMID: 26190673
- Reades R et al. Acceso vascular intraóseo versus acceso vascular intravenoso durante un paro cardíaco extrahospitalario: un ensayo controlado aleatorio. Ann EmergMed 2011; 58 (6): 509 – 16. PMID: 21856044
- Enlace MS et al. Parte 7: Soporte vital cardiovascular avanzado para adultos: Actualización de las directrices de la Asociación Estadounidense del Corazón de 2015 para reanimación cardiopulmonar y atención cardiovascular de emergencia. Circulación 2015; 132 (18 Suplemento 2): S444 – 64. PMID: 26472995
- Littmann et al. Una herramienta didáctica simplificada y estructurada para la evaluación y gestión de la actividad eléctrica sin pulso. Med Princ Pract 2014; 23 (1): 1 – 6. PMID: 23949188
- Ochoa FJ et al. Competencia de los profesionales de la salud para comprobar el pulso carotídeo. Reanimación 1998; 37: 173 – 75. PMID: 9715777
- Blyth L et al. Ecocardiografía centrada en la cabecera de la cama como predictor de supervivencia en pacientes con paro cardíaco: una revisión sistemática. Medicina Académica de Emergencia 2012; 19 (10): 1119 – 26. PMID: 23039118
- Ahrens T et al. Mediciones de dióxido de carbono al final de la espiración como indicador pronóstico del resultado en un paro cardíaco. Soy J Crit Care 2001; 10(6): 391 – 8. PMID: 11688606
- Paley J y cols. Tasas de infusión introsea bajo alta presión: una comparación cadavérica de sitios anatómicos. J Trauma Acute Care Surg 2015; 78 (2): 295 – 9. PMID: 25757113
- Benger J.R. et al. Efecto de una estrategia de un dispositivo de vía aérea supraglótica frente a la intubación traqueal durante un paro cardíaco extrahospitalario sobre el resultado funcional: ensayo clínico aleatorizado AIRWAYS-2. JAMA 2018. [ Publicación electrónica antes de la impresión ]
- Jabre P et al. Efecto de la ventilación con bolsa-mascarilla frente a la intubación endotraqueal durante la reanimación cardiopulmonar sobre el resultado neurológico después de un paro cardiorrespiratorio extrahospitalario: un ensayo clínico aleatorizado. JAMA 2018 [ Publicación electrónica antes de la impresión ]
- Perkins GD y cols. Un ensayo aleatorizado de epinefrina en paro cardíaco extrahospitalario. NEJM 2018. [ Publicación electrónica antes de la impresión ]
- Bergum D et al. Patrones de ECG en la actividad eléctrica temprana sin pulso: asociaciones con la etiología y la supervivencia del paro cardíaco intrahospitalario. Reanimación 2016. PMID: 27143124
- Gardner, KF y cols. El examen de evaluación ecográfica del paro cardíaco (CASA): un enfoque estandarizado para el uso del ultrasonido en la PEA. AJEM 2018. PMID: 28851499
Apoye el espectáculo pagando y reclamando 1,5 horas de CME/CEH haciendo clic en el logotipo a continuación
Publicación revisada por pares por: Anand Swaminathan (Twitter: @EMSwami )
La publicación Más allá del ACLS: descarga cognitiva durante un paro cardíaco apareció por primera vez en REBEL EM - Blog de medicina de emergencia .

