
 Antecedentes: El mundo ha estado involucrado en esfuerzos de vacunación masiva durante los últimos nueve meses. Desde que se aprobaron las vacunas, se han administrado miles de millones de dosis. Los ensayos iniciales demostraron que las vacunas contra la COVID-19 son eficaces y seguras. Sin embargo, evaluar la seguridad de la vacuna basándose en los ensayos de fase 3 tiene algunas limitaciones; números limitados de participantes, población de muestra más saludable que el promedio, etc. Esto hace que estos ensayos no tengan suficiente poder estadístico para identificar eventos adversos menos comunes. Los datos de la vida real posteriores al estudio han revelado una mayor aparición de algunos eventos adversos después de la vacunación, como miocarditis, trombosis, linfadenopatía, parálisis idiopática del nervio facial, etc. Estos eventos adversos pueden haber disminuido la confianza en la vacunación para algunos grupos. Se requiere vigilancia de vacunas para monitorear la seguridad de las nuevas vacunas en entornos del mundo real. Aunque la vigilancia activa puede ayudar a detectar tendencias sospechosas, la falta de un grupo de control limita la capacidad de identificar los efectos causales de la vacunación. En última instancia, la eficacia de la vacunación con ARNm contra el SARS-CoV-2 está bien establecida, pero carecemos de datos de seguridad de alta calidad en el mundo real.
Antecedentes: El mundo ha estado involucrado en esfuerzos de vacunación masiva durante los últimos nueve meses. Desde que se aprobaron las vacunas, se han administrado miles de millones de dosis. Los ensayos iniciales demostraron que las vacunas contra la COVID-19 son eficaces y seguras. Sin embargo, evaluar la seguridad de la vacuna basándose en los ensayos de fase 3 tiene algunas limitaciones; números limitados de participantes, población de muestra más saludable que el promedio, etc. Esto hace que estos ensayos no tengan suficiente poder estadístico para identificar eventos adversos menos comunes. Los datos de la vida real posteriores al estudio han revelado una mayor aparición de algunos eventos adversos después de la vacunación, como miocarditis, trombosis, linfadenopatía, parálisis idiopática del nervio facial, etc. Estos eventos adversos pueden haber disminuido la confianza en la vacunación para algunos grupos. Se requiere vigilancia de vacunas para monitorear la seguridad de las nuevas vacunas en entornos del mundo real. Aunque la vigilancia activa puede ayudar a detectar tendencias sospechosas, la falta de un grupo de control limita la capacidad de identificar los efectos causales de la vacunación. En última instancia, la eficacia de la vacunación con ARNm contra el SARS-CoV-2 está bien establecida, pero carecemos de datos de seguridad de alta calidad en el mundo real.
En mayo de 2021, aproximadamente 5 millones de personas (≈55% de la población) en Israel habían recibido dos dosis de la vacuna BNT162b2 (Pfizer). Ahora contamos con un gran conjunto de datos de una de las organizaciones de atención médica más grandes de Israel para comparar la incidencia de posibles eventos adversos entre personas vacunadas versus personas no vacunadas, así como la incidencia de eventos adversos asociados con la infección por SARS-CoV-2 (la enfermedad que estas intervenciones pretenden prevenir o tratar).
Artículo: Barda, N et al. Seguridad de la vacuna COVID-19 de ARNm BNT162b2 a nivel nacional. NEJM 2021. PMID: 34432976
Pregunta clínica: ¿Cuál es el riesgo de resultados adversos después de la vacunación contra el COVID-19 con ARNm de BNT162b2 en comparación con la infección natural por SARS-CoV-2?
Que hicieron:
- Ensayo prospectivo observacional emparejado de casos
- Caso emparejado de personas vacunadas con personas no vacunadas según variables sociodemográficas y clínicas
- De manera similar, también se compararon casos de personas infectadas por SARS-CoV-2 con personas no infectadas.
- Se derivaron los índices de riesgo y las diferencias de riesgo a los 42 días después de la vacunación.
Resultados:
- Incidencia de eventos adversos hasta 42 días después de la vacunación o infección
Inclusión:
- ≥16 años de edad
- Membresía continua en la organización de atención médica durante un año completo.
- Sin infección previa por SARS-CoV-2
- No contacto con el sistema de salud en los 7 días anteriores (Este criterio se incluyó como indicador de un evento de salud no relacionado con la vacunación posterior que podría reducir la probabilidad de recibir la vacuna)
Exclusión:
- Poblaciones en las que no se pudieron abordar adecuadamente los factores de confusión
- Residentes de centros de atención a largo plazo
- Confinados en domicilios por motivos médicos
- trabajadores de la salud
- Faltaban datos sobre el índice de masa corporal o la zona residencial
Resultados:
- 884.828 mil personas en cada grupo (Vacunados vs No vacunados)
- El 4% de las personas elegibles fueron emparejadas exitosamente
- Edad media de la cohorte = 38 años
- Sexo femenino = 48%
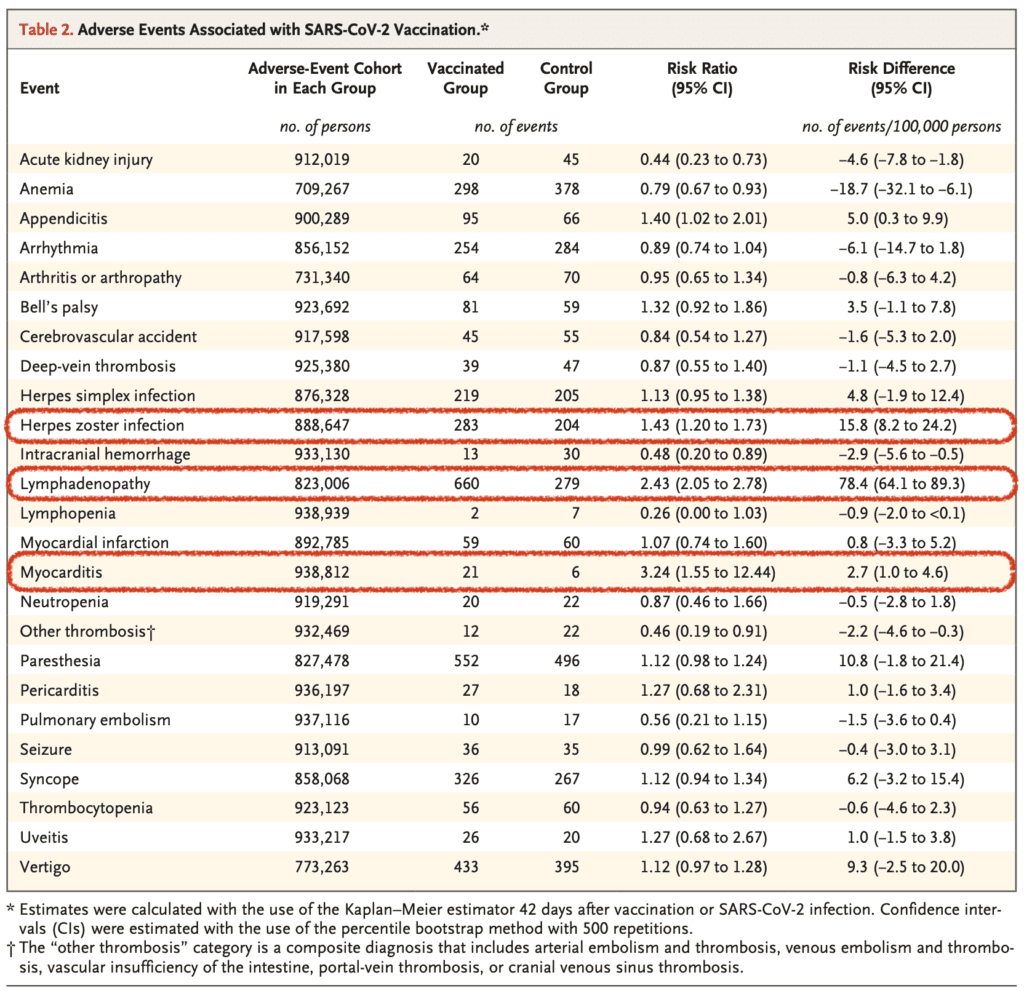
- Los 3 efectos adversos más comunes observados en poblaciones vacunadas y no vacunadas:
- Miocarditis: la incidencia fue mayor después de la segunda vacunación
- Linfadenopatía
- Apendicitis
- Infección por herpes zóster
- La vacunación, en comparación con ninguna vacunación, protegió más contra:
- Anemia
- Lesión renal aguda
- Hemorragia intracraneal
- Linfopenia
- 173,106 personas en cada grupo (Infección versus No Infección)
- El 8% de las personas elegibles fueron emparejadas exitosamente
- Edad media de la cohorte = 34 años
- Sexo femenino = 54%
- Comparación de vacunados y no vacunados con infección o sin infección
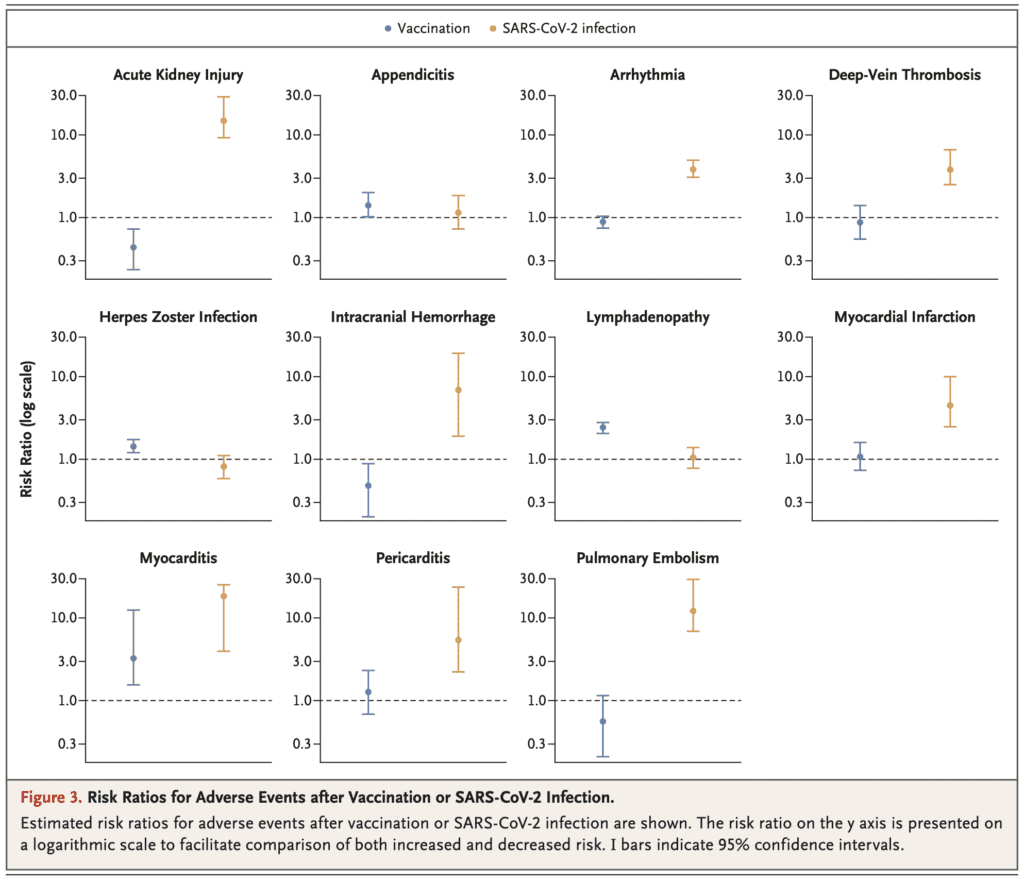
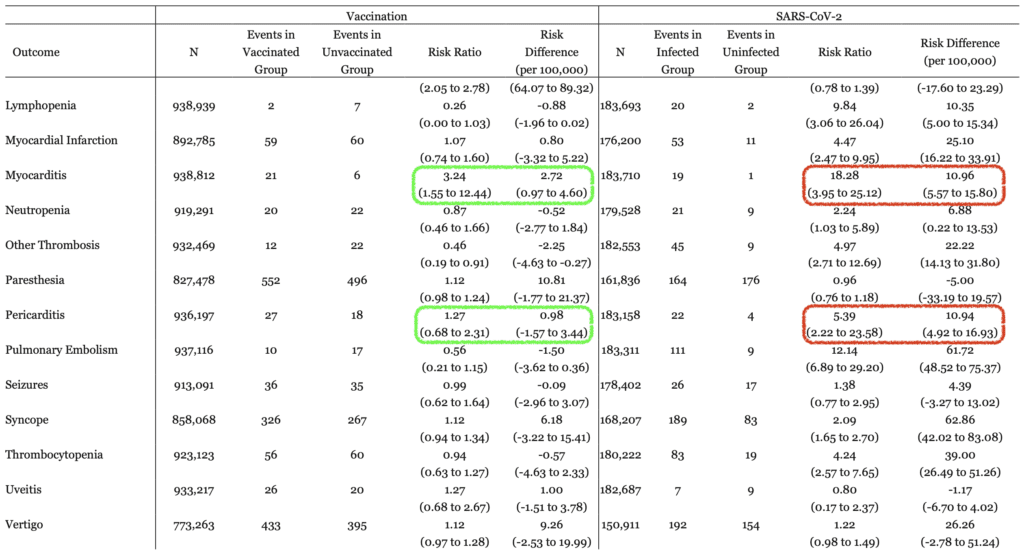
- Al observar específicamente el resultado de la miocarditis, hubo un riesgo significativamente mayor de contraer miocarditis en pacientes que no estaban vacunados y adquirieron la infección por SARS-CoV-2.
- Miocarditis:
- Vacunados RR 3.24
- Diferencia de riesgo entre vacunados y no vacunados 2,72
- Infección por SARS-CoV-2 RR 18,28
- Diferencia de riesgo entre SARS-CoV-2 y sin SARS-Co-V-2 10,96
- Miocarditis:
Fortalezas:
- Hace una pregunta clínicamente importante.
- Se utilizó una base de datos grande y completamente digitalizada (≈50% de la población) para evaluar una amplia gama de posibles eventos adversos.
- Se intentó emular una asignación aleatoria haciendo coincidir exactamente a personas vacunadas y no vacunadas en un conjunto de variables de referencia que se consideraban posibles factores de confusión.
- No hay financiación comercial para el estudio.
- Se elaboró una lista de posibles eventos adversos de múltiples fuentes (es decir, VAERS, BEST y SPEAC, fabricante de vacunas y publicaciones científicas relevantes).
- Proporcionó un contexto de riesgo de eventos adversos causados por la vacuna BNT162b2 en comparación con eventos adversos después de una infección documentada con SARS-CoV-2.
Limitaciones:
- Los efectos de la vacunación y la infección por SARS-CoV-2 se estimaron con diferentes composiciones de cohortes, por lo que los resultados de los conjuntos separados son difíciles de comparar directamente (es decir, vacunación frente a no vacunación e infectados frente a no infectados).
- Se excluyeron algunos grupos de alto riesgo (es decir, trabajadores de la salud, residentes en centros de atención a largo plazo) que tienen un mayor riesgo de sufrir eventos adversos.
- Es posible que las personas con mayor conciencia clínica (es decir, las que se vacunan o después de la infección por SARS-CoV-2) tengan más probabilidades de informar o buscar atención médica por sus síntomas, lo que da como resultado una sobreestimación de la incidencia de diversos eventos adversos en el grupos vacunados o infectados
- Los eventos adversos como el riesgo de transmisión a miembros de la familia quedaron fuera del alcance de este estudio.
Discusión:
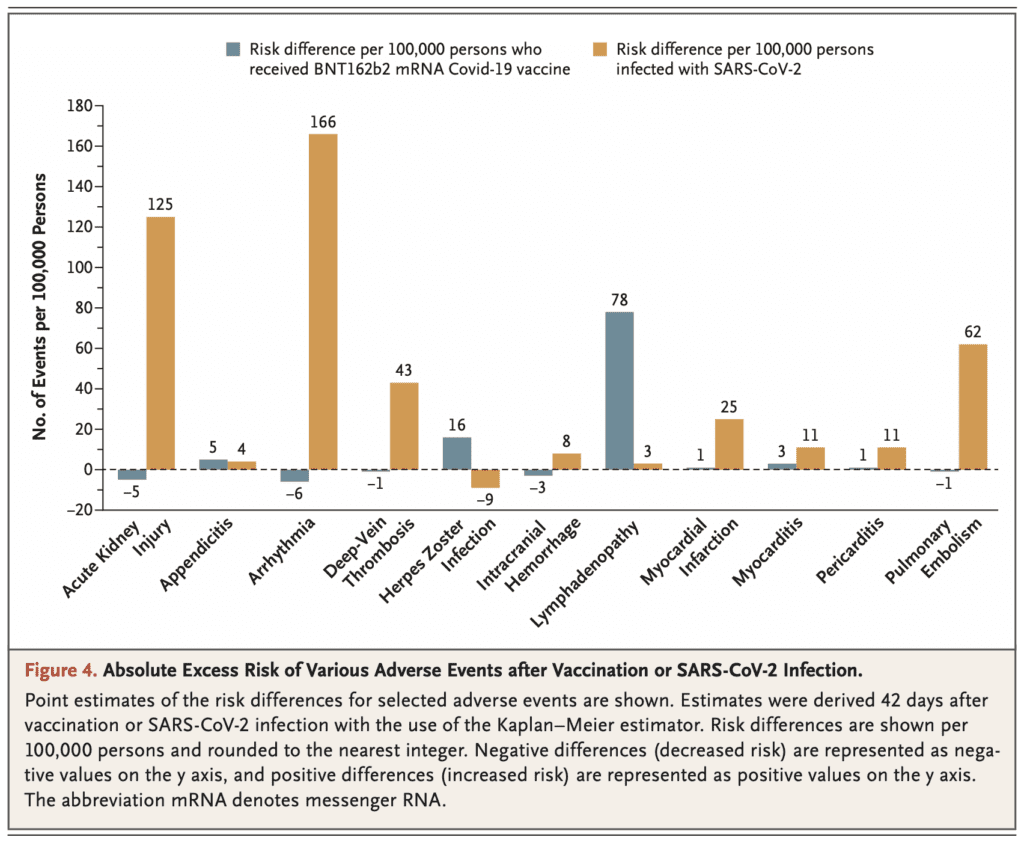
- Los principales eventos adversos potenciales asociados con la vacunación identificados incluyeron un riesgo excesivo de:
- Linfadenopatía: 78,4 eventos por 100.000 personas
- Infección por herpes zóster: 15,8 eventos por 100.000 personas
- Apendicitis: 5,0 eventos por 100.000 personas
- Miocarditis: 2,7 eventos por 100.000 personas
- Para poner en contexto los posibles eventos adversos asociados con la vacunación, es importante observar los eventos adversos en personas con infección por SARS-CoV-2:
- No se estimó que la infección tuviera un efecto significativo sobre la incidencia de linfadenopatía, infección por herpes zóster o apendicitis.
- Sin embargo, se estimó que la infección por SARS-CoV-2 daba como resultado un riesgo excesivo sustancial de miocarditis (11,0 eventos por 100.000 personas)
- Además, se descubrió que la infección por SARS-CoV-2 aumenta sustancialmente el riesgo de varios eventos adversos para los cuales no se encontró que la vacunación aumentara:
- Arritmia: 166,1 eventos por 100.000
- Lesión renal aguda: 125,4 eventos por 100.000
- Embolia pulmonar: 61,7 eventos por 100.000
- TVP: 43,0 eventos por 100.000
- Infarto de miocardio: 25,1 eventos por 100.000
- Pericarditis: 10,9 eventos por 100.000
- Hemorragia intracraneal: 7,6 eventos por 100.000
- El riesgo de miocarditis fue significativamente mayor con la infección natural por SARS-CoV-2 (11 eventos por 100 000 personas) que con la vacunación contra el SARS-CoV-2 (3 eventos por 100 000 personas):
- Vacunación: 3 eventos en exceso por cada 100.000 vacunas
- IC del 95%: 1 a 5 eventos excesivos por 100 000 vacunaciones
- La edad media fue de 25 años (rango de 20 a 34)
- 9% eran hombres
Conclusión del autor: “En este estudio realizado en un entorno de vacunación masiva a nivel nacional, la vacuna BNT162b2 no se asoció con un riesgo elevado de la mayoría de los eventos adversos examinados. La vacuna se asoció con un riesgo excesivo de miocarditis (de 1 a 5 eventos por 100.000 personas). El riesgo de este evento adverso potencialmente grave y de muchos otros eventos adversos graves aumentó sustancialmente después de la infección por SARS-CoV-2”.
Punto clínico para recordar: La vacuna BNT162b2 (Pfizer) para el SARS-CoV-2 da como resultado un ligero aumento en la incidencia de eventos adversos durante un período de seguimiento de 42 días. Sin embargo, la mayoría de los efectos adversos son de naturaleza leve. La miocarditis, que se considera un evento adverso potencialmente grave, tuvo una mayor incidencia con la vacunación (3 eventos por cada 100 000 vacunas), PERO la infección por SARS-CoV-2 en sí misma fue un riesgo mayor de miocarditis (11 eventos por 100 000 infecciones).
Referencias:
- Barda, N y cols. Seguridad de la vacuna COVID-19 de ARNm BNT162b2 a nivel nacional. NEJM 2021. PMID: 34432976
Publicación revisada por pares por: Anand Swaminathan, MD (Twitter: @EMSwami )
La publicación Todo es cuestión de riesgo: vacunación contra el COVID-19 con ARNm de BNT162b2 versus infección natural apareció por primera vez en REBEL EM - Blog de medicina de emergencia .
