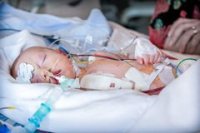
 Al igual que en los adultos, la sepsis pediátrica es un tema complejo que requiere investigaciones continuas. En los Estados Unidos, se estima que hay 75.000 casos por año de sepsis pediátrica grave con una mortalidad hospitalaria del 5 al 10%. 1,2 Esta es una de las afecciones más mortales tratadas en niños. Además, después del caso de Rory Staunton , el estado de Nueva York aprobó regulaciones que exigen que todos los hospitales tengan sistemas de reconocimiento, tratamiento y notificación de datos específicos para pediatría. Varios otros estados han adoptado, o están considerando, requisitos similares. Por tanto, es fundamental que los médicos de urgencias comprendan al menos los conceptos básicos del tratamiento de la sepsis pediátrica.
Al igual que en los adultos, la sepsis pediátrica es un tema complejo que requiere investigaciones continuas. En los Estados Unidos, se estima que hay 75.000 casos por año de sepsis pediátrica grave con una mortalidad hospitalaria del 5 al 10%. 1,2 Esta es una de las afecciones más mortales tratadas en niños. Además, después del caso de Rory Staunton , el estado de Nueva York aprobó regulaciones que exigen que todos los hospitales tengan sistemas de reconocimiento, tratamiento y notificación de datos específicos para pediatría. Varios otros estados han adoptado, o están considerando, requisitos similares. Por tanto, es fundamental que los médicos de urgencias comprendan al menos los conceptos básicos del tratamiento de la sepsis pediátrica.
Definición de sepsis
Ha habido muchas y variadas definiciones de sepsis y, al igual que con los criterios actualizados para adultos, es probable que cambien tres definiciones pediátricas. Para este artículo:
Sepsis = Disfunción del sistema orgánico + Infección
 Líquidos intravenosos
Líquidos intravenosos
Aunque uno podría pensar que los líquidos son el primer tratamiento para la mayoría de los tipos de shock, la reanimación con líquidos en la sepsis pediátrica es controvertida.
En pacientes adultos, los ensayos ProCESS, 4 ARISE, 5 y PromISE 6 no lograron demostrar un beneficio en la mortalidad de la atención estricta basada en protocolos versus la atención “habitual”. Desafortunadamente, hay pocos datos pediátricos para continuar. Pero, curiosamente, un artículo de Maitland mostró un efecto NOCIVO de los bolos de líquido en niños africanos con sepsis. 7
¿Significa esto que debemos restringir los líquidos a todos nuestros pacientes?
Aunque un artículo no refuta todo el conocimiento existente sobre los fluidos y la sepsis, SÍ plantea preguntas. Las pautas de soporte vital avanzado pediátrico (PALS) de 2015 proporcionaron un resumen de la evidencia disponible para la reanimación con líquidos (reproducida a continuación), y la mayoría de los estudios no logran mostrar un beneficio. 8
| Supervivencia hasta el alta hospitalaria | Necesidad de transfusión o diuréticos | Necesidad de líquido de rescate | Ventilador Mecánico o Vasopresor | Tiempo hasta la resolución del shock | Líquidos intravenosos totales | |
| Sepsis grave/choque séptico | Ningún beneficio 9,10 | Sin beneficio | No hay estudios disponibles | Sin beneficio | Sin beneficio | No hay estudios disponibles |
| Malaria grave | Sin beneficio 11 | Sin beneficio | Dañar | No hay estudios disponibles | Sin beneficio | Sin beneficio |
| Enfermedad febril grave (con algunos signos de shock) | Beneficio 7,12 | Sin beneficio | No hay estudios disponibles | No hay estudios disponibles | Dañar | Sin beneficio |
Tabla 1. Evidencia del uso de volumen restrictivo de reanimación con líquidos intravenosos, en comparación con volumen no restrictivo, según la enfermedad de presentación y el resultado en pacientes pediátricos. 8
Recomendaciones de la campaña PALS y Surviving Sepsis sobre líquidos intravenosos
El algoritmo PALS actualizado de 2015 sugiere las siguientes pautas con cierta ambigüedad, probablemente debido a la escasez de literatura existente:
| Recomendación PALS | Nuestro comentario |
| Administre bolos de líquido de 20 ml/kg (cristaloide isotónico) IV/IO durante 5 a 20 minutos o más rápido si es necesario. | Pero, ¿es más rápido necesariamente mejor? |
| Repita el bolo de líquidos de 20 ml/kg (hasta 60 ml/kg) hasta que los síntomas clínicos mejoren o el paciente desarrolle signos de sobrecarga de líquidos. | |
| Puede seguir requiriendo líquidos adicionales por encima de 60 ml/kg. | Espera, ¿no acaban de decir hasta 60 ml/kg? Interpretación: Cuando empiece a superar este total, considere intervenciones adicionales o diagnósticos alternativos . |
| El volumen de reanimación con líquidos puede acercarse a 200 ml/kg en el shock séptico caliente. | ¡Eso podría ser hasta 10 bolos! |
Tabla 2. Recomendaciones de la campaña PALS y Surviving Sepsis de 2015 sobre líquidos intravenosos con comentarios
La campaña Surviving Sepsis tiene solo 3 páginas sobre sepsis pediátrica y establece explícitamente que se deben seguir las pautas de PALS. 13 La directriz existente de la Sociedad de Medicina de Cuidados Críticos (SCCM), que se actualizó por última vez en 2009, 14 aborda este enigma:
La infusión de líquido se inicia mejor con bolos de 20 ml/kg, titulados para asegurar una presión arterial adecuada y monitores clínicos del gasto cardíaco, incluida la frecuencia cardíaca, la calidad de los pulsos periféricos, el llenado capilar, el nivel de conciencia, la temperatura de la piel periférica y la producción de orina. 14
Además, no existe una elección clara sobre “el mejor” fluido. Utilice el cristaloide isotónico de su elección, pero tenga en cuenta que puede haber subconjuntos de pacientes para quienes la albúmina puede ser apropiada. ¡Se avecinan más investigaciones!
Conclusión en líquidos intravenososNO siga protocolos estrictos que exijan volúmenes mínimos de líquido para pacientes con sepsis. Es mejor realizar reevaluaciones frecuentes y adaptar el volumen de reanimación con líquidos a cada paciente individual. |

antibióticos
Este es uno de los lugares donde saber qué hacer puede ser fácil y lograrlo resulta difícil.
En 2014 Weiss et al. evaluaron pacientes pediátricos en un hospital pediátrico de atención terciaria que fueron tratados por sepsis grave o shock séptico. En los pacientes que reciben el primer antibiótico apropiado más de 3 horas después de cumplir los criterios de sepsis grave o shock séptico, el OR de mortalidad en UCIP ajustado fue de 4,84 (1,45 – 16,2) en comparación con los pacientes que recibieron antibióticos en menos de 3 horas . Sin embargo, el tiempo medio para recibir el primer antimicrobiano fue de 140 minutos (¡más de 2 horas!) y se hace eco de un artículo de Paul et al 15 que muestra un cumplimiento deficiente de los objetivos de sincronización de los antibióticos. La mayor parte del retraso se debió al pedido hasta la entrega de antibióticos, en lugar de recibir los pedidos. Hay muchos lugares a los que se podría atribuir este retraso, como el acceso intravenoso, la preparación de medicamentos, la entrega desde la farmacia y la instalación de la bomba intravenosa. En cada institución, los impulsores son diferentes.
Si bien todos nos esforzamos por lograr una administración de antibióticos y una menor incidencia de resistencia, estos no son los pacientes a los que debemos dirigir esos esfuerzos. Piense en la frecuencia con la que se administra amoxicilina para la otitis media y luego aplique al menos una primera dosis de antibióticos a sus pacientes potencialmente sépticos lo más rápido posible. Asegúrese de que todos los involucrados en la atención de ese paciente sepan lo importante que es la velocidad.
Conclusión sobre los antibióticosPara sus pacientes potencialmente sépticos, decida cuáles son los antibióticos adecuados y administre la primera dosis lo antes posible. |
 Vasopresores
Vasopresores
Nuevamente los datos pediátricos son limitados. Las directrices de la SSCM enumeran la dopamina como el vasoactivo de primera línea para la sepsis pediátrica en la mayoría de los casos. En la actualización de PALS de 2015, todavía se recomienda la clasificación del shock séptico mediante la medición de ScVO2 y la definición clásica de shock “cálido” y “frío” para determinar la elección vasoactiva. En la práctica, particularmente en el servicio de urgencias, muy pocos pacientes pediátricos tienen mediciones de ScVO2, y tenemos evidencia de que no somos tan buenos para clasificar el shock de calor versus el de frío como pensamos 16 . Varios estudios en adultos mostraron una mayor mortalidad con dopamina en comparación con otros agentes vasoactivos.
qué hacemos?
Sólo disponemos de un ensayo pediátrico, que comparó la dopamina con la epinefrina en estos pacientes, 17 que mostró un aumento de la mortalidad y la morbilidad con la dopamina. Existen algunas dudas sobre si las dosis de los medicamentos utilizados en este ensayo son realmente equivalentes. Hasta el momento no hay una respuesta definitiva disponible, aunque la SCCM debe publicar directrices actualizadas sobre este tema. En la práctica, la dopamina suele ser el medicamento vasoactivo que se inicia más rápidamente en el servicio de urgencias pediátrico, pero la transición de estos pacientes a norepinefrina o epinefrina debe realizarse rápidamente.
Una nota sobre los esteroides: no están indicados de forma rutinaria, pero son una opción para pacientes refractarios a líquidos y medicamentos vasoactivos, o que tienen riesgo de insuficiencia suprarrenal.
Conclusión sobre los vasopresoresPiense en vasopresores para cualquier paciente que no responda a su tercer bolo de líquido intravenoso y prepare alguna otra intervención. Para empezar, la dopamina está bien, pero conviene pensar en hacer una transición rápida a un fármaco diferente. Los esteroides no están indicados de forma rutinaria, pero si el paciente no responde a los vasopresores, considere administrarlos. |
 lactato
lactato
Una vez más, los datos pediátricos son escasos. En 2012, Scott et al. demostraron que entre los pacientes pediátricos con SIRS, aquellos con lactato sérico ≥4 mmol/L en la presentación inicial, tenían más probabilidades de desarrollar disfunción orgánica, requerir ingreso en la UCI y tener enfermedades bacterianas graves. En 2016, Scott et al. evaluaron prospectivamente los niveles de lactato a las 0, 2 y 4 horas en pacientes con infección y disfunción orgánica. Los pacientes que tuvieron una normalización de sus lactatos (<2 mmol/L) tuvieron un menor riesgo de disfunción orgánica persistente a las 48 horas (RR 0,46, 0,29-0,73). En 2017, Scott et al. evaluaron la mortalidad hospitalaria a 30 días de pacientes pediátricos con sepsis y un lactato sérico >4 mmol/L. Los pacientes con niveles elevados de lactato tuvieron un OR ajustado de mortalidad de 3,26 (1,16 – 9,16). Sin embargo, pocos pacientes tenían un lactato tan alto (105 de 1299) y sólo 5 de las 25 muertes en la cohorte tenían un lactato por encima de este umbral, lo que lleva a una sensibilidad del 20% para la mortalidad a 30 días.
Conclusión sobre el lactatoEl lactato es una herramienta, entre muchas, para identificar pacientes con sepsis, pero su sensibilidad y especificidad son bajas. Los pacientes con un nivel elevado de lactato (>4 mmol/L) tienen un mayor riesgo de sufrir resultados graves, incluida la muerte. El lactato puede ser útil como marcador de estratificación del riesgo. |
 Intubación endotraqueal
Intubación endotraqueal
A menos que no puedan oxigenar, ventilar o proteger sus vías respiratorias, pocos pacientes con sepsis pediátrica requerirán intubación en el servicio de urgencias. Si pueden beneficiarse o no de la disminución de la demanda metabólica es una discusión diferente. Particularmente en pacientes con shock, que probablemente tengan una deficiencia relativa de catecolaminas y problemas con el volumen y la distribución de líquidos, los cambios fisiológicos asociados con la ventilación con presión positiva son increíblemente peligrosos. Es probable que precipite un colapso cardiovascular. Incluso en los pacientes que eventualmente requerirán intubación, lo ideal es reanimarlos primero con líquidos y tomar vasopresores, o estar preparado para iniciarlos inmediatamente, antes de hacerlo. Prepárese suponiendo que cada uno de estos pacientes sufrirá un colapso hemodinámico tras la intubación.
Resumen para el tratamiento de la sepsis pediátrica
- Las definiciones y directrices son confusas, escasas y cambiantes.
- Reevaluar a cada paciente después de cada intervención, antes de proporcionar terapias adicionales.
- La administración oportuna de líquidos intravenosos y antibióticos es fundamental.
- Comience la reanimación con líquidos rápidamente, pero no obligue a los pacientes a recibir una cantidad “mínima” de bolos. Adaptar el abordaje a cada paciente, con reevaluaciones frecuentes.
- Inicie el tratamiento con antibióticos lo antes posible y no se preocupe tanto por la administración. Si es probable que se produzca sepsis, adminístreles la primera dosis y resuelva los detalles más adelante.
- La mejor opción, el vasopresor de primera línea, probablemente no sea la dopamina. Sin embargo, en la práctica, otros vasopresores (especialmente la noradrenalina) pueden tardar más en prepararse, por lo que un enfoque razonable es comenzar con dopamina mientras prepara los otros medicamentos.
- Si el paciente permanece en shock a pesar de los líquidos intravenosos y los vasopresores, considere agregar esteroides.
- La intubación puede ser mortal y rara vez es necesaria en estos pacientes. Optimice la hemodinámica primero. Si la intubación es absolutamente necesaria, prepárese para un colapso cardiovascular.
Información del autor
La publicación PEM Pearls: Manejo de la sepsis pediátrica: comprensión de los conceptos básicos apareció por primera vez en ALiEM .

