 Antecedentes: los ensayos clínicos aleatorios que evalúan la eficacia de los corticosteroides complementarios en el shock séptico han mostrado pruebas contradictorias de relevancia clínica. Dos ensayos en particular [2][3] analizaron dosis más bajas de hidrocortisona (200 mg/día) y su efecto sobre la mortalidad en pacientes con shock séptico, lo que dio lugar a resultados contradictorios con respecto a la mortalidad, pero ambos mostraron una reversión más temprana del shock en pacientes tratados con hidrocortisona. Las guías actuales de sepsis para sobrevivientes recomiendan el uso de hidrocortisona en pacientes con shock séptico después de una reanimación adecuada con líquidos y el uso de vasopresores que no han logrado estabilidad hemodinámica, pero esta recomendación se clasifica como evidencia débil (Nivel 2C). Debido a estas recomendaciones débiles, ha habido variabilidad en el uso de corticosteroides en el shock séptico. El 19 de enero de 2018 se publicaron los resultados del ensayo ADRENAL intentando responder de una vez por todas a la pregunta de los esteroides complementarios en el shock séptico.
Antecedentes: los ensayos clínicos aleatorios que evalúan la eficacia de los corticosteroides complementarios en el shock séptico han mostrado pruebas contradictorias de relevancia clínica. Dos ensayos en particular [2][3] analizaron dosis más bajas de hidrocortisona (200 mg/día) y su efecto sobre la mortalidad en pacientes con shock séptico, lo que dio lugar a resultados contradictorios con respecto a la mortalidad, pero ambos mostraron una reversión más temprana del shock en pacientes tratados con hidrocortisona. Las guías actuales de sepsis para sobrevivientes recomiendan el uso de hidrocortisona en pacientes con shock séptico después de una reanimación adecuada con líquidos y el uso de vasopresores que no han logrado estabilidad hemodinámica, pero esta recomendación se clasifica como evidencia débil (Nivel 2C). Debido a estas recomendaciones débiles, ha habido variabilidad en el uso de corticosteroides en el shock séptico. El 19 de enero de 2018 se publicaron los resultados del ensayo ADRENAL intentando responder de una vez por todas a la pregunta de los esteroides complementarios en el shock séptico.
Que hicieron:
- Ensayo internacional, pragmático, doble ciego, aleatorizado y controlado de grupos paralelos de 3800 pacientes con shock séptico sometidos a ventilación mecánica
- Infusión de hidrocortisona (a dosis de 200 mg/día) o placebo durante 7 días o hasta la muerte o el alta de la UCI
- ADRENAL = AD conjunto con corticosteroides t RE tratamiento en pacientes críticos con shock séptico
- Intentó responder a la pregunta de si la terapia con hidrocortisona reduce la mortalidad en pacientes ingresados en UCI con shock séptico.
Resultados:
- Primario: mortalidad a 90 días
- Secundario:
- Mortalidad a los 28 días.
- Tiempo hasta la resolución del shock
- Recurrencia del shock
- Duración de la estancia en la UCI
- Duración de la estancia hospitalaria
- Frecuencia y duración de la ventilación mecánica.
- Frecuencia y duración del tratamiento con terapia de reemplazo renal.
- Incidencia de bacteriemia o fungemia de nueva aparición entre 2 y 14 días después de la aleatorización
- Requisitos de transfusión de sangre
Inclusión:
- Adultos (≥18 años de edad) sometidos a ventilación mecánica con fuerte sospecha clínica de infección, que cumplieron 2 o más criterios de SRIS
- Vasopresores continuos o inotrópicos para mantener una PAS >90 mmHg o una PAM media >60 mmHg, o una PAM objetivo establecida por el médico tratante para mantener la perfusión.
- Administración de vasopresores o inotrópicos durante ≥4 horas y presentes en el momento de la aleatorización
Exclusión:
- Recibir corticosteroides sistémicos por una indicación distinta del shock séptico
- Etomidato recibido
- Pacientes que reciben tratamiento con anfotericina B para infecciones fúngicas sistémicas en el momento de la aleatorización
- Pacientes con malaria cerebral documentada.
- Pacientes con infección documentada por Strongyloides.
- Se considera que sufre la muerte dentro de los 90 días debido a una enfermedad preexistente.
- Limitaciones de tratamiento vigentes (es decir, DNR)
- Cumplió todos los criterios de inclusión durante >24 horas
Resultados:
- 3.800 pacientes de 69 UCI médico-quirúrgicas fueron aleatorizados
- Se incluyeron 3658 pacientes en el resultado primario.
- 1832 pacientes en el grupo de hidrocortisona
- 1826 pacientes en el grupo placebo
- Desglose del tipo de admisión:
- No operatorio (médico) ≈ 68%
- Operativo (Quirúrgico) ≈ 32%
- Todos los pacientes recibieron un tratamiento inicial similar:
- Ventilación Mecánica ≈ 100%
- Inótropos/Vasopresores ≈ 100%
- Antimicrobianos ≈ 98%
-
Muerte por cualquier causa a los 90 días (resultado primario):
- Grupo Hidrocortisona: 27,9%
- Grupo placebo: 28,8%
- OR 0,95; IC del 95 %: 0,82 – 1,10; p = 0,50
- El 7 % de los pacientes recibieron esteroides abiertos, pero después de realizar un análisis post hoc del resultado primario excluyendo a estos pacientes, todavía no hay diferencias en la mortalidad OR 0,96; IC del 95 %: 0,82 – 1,12; p = 0,59
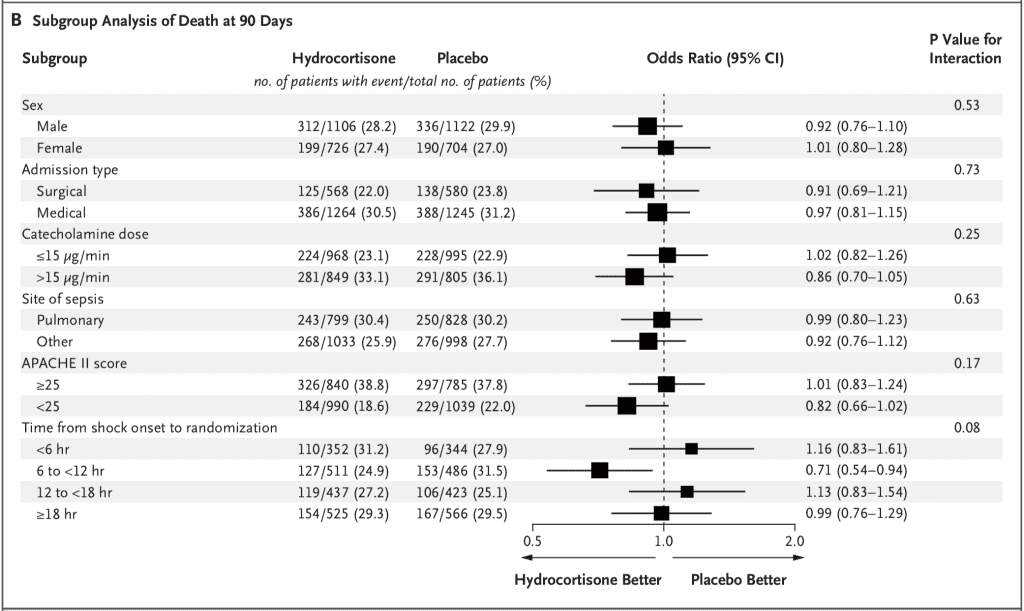
- Tampoco hubo diferencias en la mortalidad entre 6 subgrupos preespecificados:
- Se incluyeron 3658 pacientes en el resultado primario.
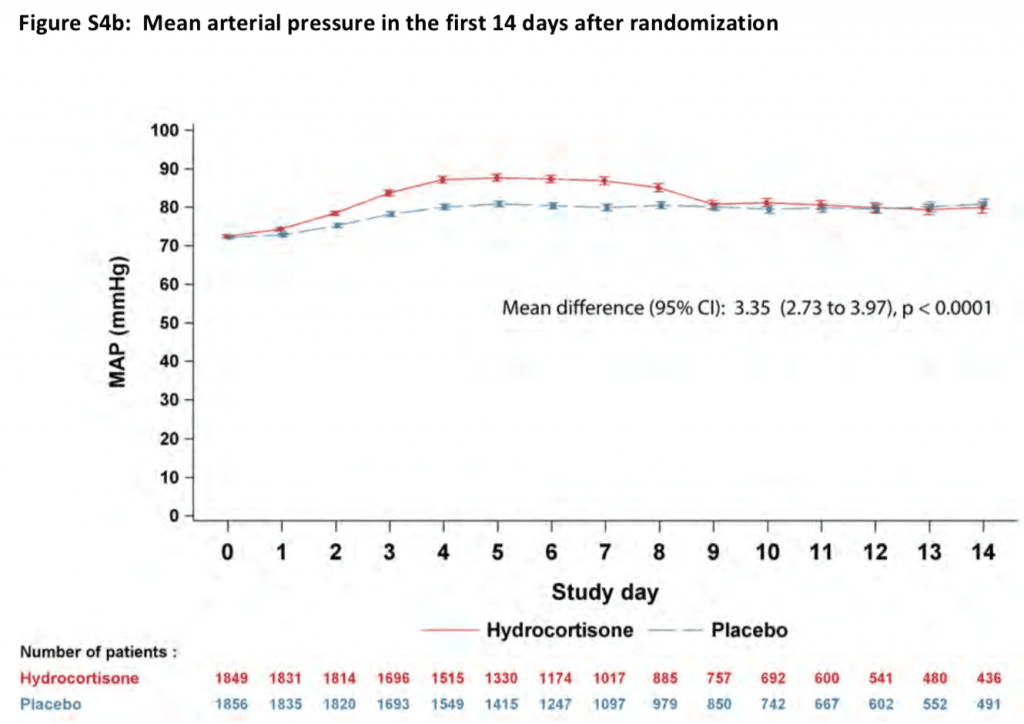
- Tiempo medio hasta la reversión del shock
- Grupo de hidrocortisona: 3 días (rango 2 – 5)
- Grupo placebo: 4 días (rango 2 – 9)
- HR 1,32; IC del 95 %: 1,23 – 1,41; p<0,001
- No hay diferencia estadística en:
- Mortalidad a los 28 días
- Tasa de recurrencia del shock.
- Número de días vivos y fuera de la UCI
- Número de días vivos y fuera del hospital
- Recurrencia de la ventilación mecánica.
- Tasa de terapia de reemplazo renal
- Incidencia de bacteriemia o fungemia de nueva aparición
- Eventos adversos
- Total de 33 eventos adversos
- Grupo Hidrocortisona: 1% (24 eventos)
- Grupo Placebo: 0,3% (3 eventos)
- P = 0,009
- hiperglucemia
- Hidrocortisona: 6 eventos
- Placebo 3 Eventos
- Eventos adversos graves
- Grupo Hidrocortisona: 4 Eventos
- Grupo placebo: 2 eventos
Fortalezas:
- Un ensayo internacional, pragmático, doble ciego, aleatorizado y controlado con grupos paralelos aumenta la validez de los resultados
- Resultado primario clínicamente importante y centrado en el paciente.
- Las poblaciones más grandes de pacientes con shock séptico se incluirán en un ensayo que responda a la pregunta sobre los corticosteroides complementarios en el shock séptico (es decir, 3800 pacientes).
- Ensayo Annane [2]: 3,5 años para inscribir a 299 pacientes
- Ensayo CORTICUS [3]: 3,5 años para inscribir a 499 pacientes
- Ensayo VASST: 5 años para inscribir a 778 pacientes
- Ensayo APROCCHS: 6,9 años para inscribir a 1241 pacientes
- Ensayo ADRENAL: 4,1 años para inscribir a 3.800 pacientes
- Incluso antes de que se completara el ensayo, se publicó el protocolo del ensayo y el plan de análisis estadístico para ayudar a reducir el sesgo en los resultados.
- Ni Pfizer (que suministra hidrocortisona) ni Radpharm Scientific (que suministra placebo) participaron en el diseño o la realización del estudio, la recopilación de datos, el análisis estadístico o la redacción del manuscrito.
- Aleatorizaciones ocultas mediante una interfaz basada en web, cifrada y protegida con contraseña
- Los pacientes, los médicos tratantes y el personal del ensayo estaban cegados con respecto a la hidrocortisona frente al placebo, que se completó mediante el uso de viales enmascarados idénticos.

- Resultado primario examinado en 6 subgrupos preespecificados para garantizar que ningún subgrupo se beneficiaría de la terapia con hidrocortisona.
- Un estadístico independiente realizó dos análisis intermedios cuando se pudo evaluar a 950 pacientes (25 % de la inscripción) y 2500 pacientes (66 % de la inscripción) con respecto al resultado primario.
- Las características iniciales de los pacientes fueron similares. En otras palabras, una población de pacientes no estaba más enferma que la otra.
- Muy pocos pacientes se perdieron durante el seguimiento (28 pacientes o 0,7% de la población del estudio), lo que aumenta la validez de los resultados.
- Resultados verificados en 5 sistemas hospitalarios diferentes, lo que aumenta la validez externa para la práctica general.
Limitaciones:
- Los pacientes que recibieron etomidato fueron excluidos de este estudio. Sin embargo, es posible que muchos proveedores todavía estén usando etomidato para las LER en pacientes sépticos.
- Los eventos adversos se registraron según el criterio del médico como relacionados con el régimen del ensayo, pero este criterio no se resolvió.
- No se recopilaron datos sobre todas las infecciones secundarias.
- Tampoco se resolvió la idoneidad de la terapia con antibióticos.
- Se utilizaron tasas de ventilación recurrente como sustituto de la miopatía, pero no se evaluó la debilidad neuromuscular a largo plazo.
- No se realizó un análisis detallado de costos y beneficios.
- No está claro qué cantidad de líquido recibieron los pacientes en cada brazo del estudio, ya que demasiado líquido se ha asociado con una mayor mortalidad.
- Es posible que exista una diferencia significativa para un resultado más pequeño pero aún clínicamente relevante (es decir, la diferencia del 0,9% podría ser real si se reclutara un grupo más grande y, en un gran número de pacientes, aún podría ser importante)
- El tratamiento sin esteroides queda a criterio del médico tratante, aunque según los autores el tratamiento siguió las directrices de la MBE para la sepsis.
Discusión:
- Este ensayo fue diferente de muchos otros ensayos que intentaron responder esta pregunta, ya que utilizaron una infusión de hidrocortisona de 200 mg/día en lugar de una dosis en bolo.
- No se realizaron pruebas de corticotropina debido a la naturaleza controvertida de los resultados de estas pruebas en pacientes críticamente enfermos.
- Desglose de la mortalidad a 90 días por región inscrita (la mayoría de los inscritos procedieron de Australia ≈ 70%)
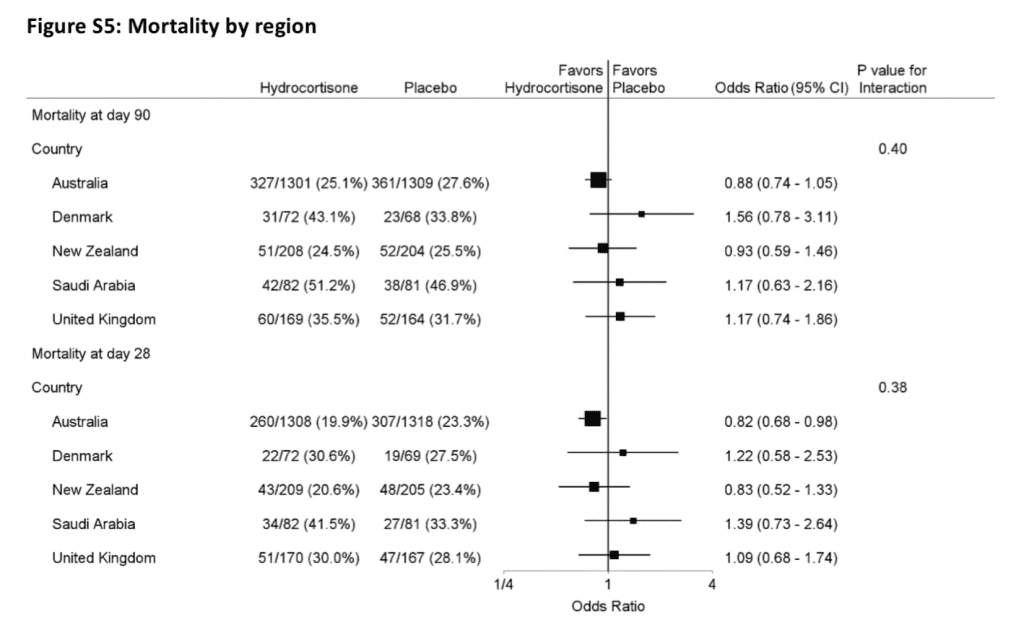
- La mayoría de los sitios de infección fueron:
- Pulmonar: 33,8% grupo Hidrocortisona y 36,5% grupo Placebo
- Abdominal: 25,9% grupo Hidrocortisona y 25,2% grupo Placebo
- Algunos puntos interesantes a considerar (y no estoy seguro de que tengamos las respuestas a estas preguntas):
- ¿Es mejor la infusión que el bolo?
- ¿La duración adecuada es de 7 días?
Conclusión del autor: "Entre los pacientes con shock séptico sometidos a ventilación mecánica, una infusión continua de hidrocortisona no resultó en una mortalidad a 90 días menor que el placebo".
Punto clínico para recordar: Sin embargo, en pacientes con shock séptico, ingresados en la UCI con ventilación mecánica y que requieren ≥4 horas de vasopresores/inotrópicos, la infusión de hidrocortisona (200 mg/d) en comparación con el placebo no marca una diferencia en la mortalidad a 90 días. hubo algunos resultados secundarios mejorados que incluyen: reversión del shock, días sin ventilador, estancia en la UCI y menos transfusiones de sangre requeridas (el último es una hipótesis que genera, según lo afirmado por los autores).
Referencias:
- Venkatesh B et al. Terapia complementaria con glucocorticoides en pacientes con shock séptico. NEJM 2018. [ Publicación electrónica antes de la impresión ]
- Annane D et al. Efecto del tratamiento con dosis bajas de hidrocortisona y fludrocortisona sobre la mortalidad en pacientes con shock séptico. JAMA 2002. PMID: 12186604
- Sprung CL et al. Tratamiento con hidrocortisona para los pacientes con shock séptico. El ensayo CORTICUS. NEJM 2008. PMID: 18184957
Para obtener más ideas sobre este tema, consulte:
- Ryan Radecki en EM Literature of Note: La palabra definitiva sobre esteroides en el shock séptico
- David Slessor en The Bottom Line: Tratamiento complementario con corticosteroides en pacientes críticamente enfermos con shock séptico
- Rory Spiegel en EMNerd (EMCrit): El caso de la insuficiencia relativa
- Dan Horner en el blog de St. Emlyn: ¿El fin del 'Roid?'
- Josh Farkas en PulmCrit (EMCrit): Reanimación de la sepsis metabólica: golpe fuerte, golpe rápido, sin remordimientos
- Mike Winters en Resuscitation: Episodio 89 – ¿Esteroides en shock séptico? ¿Finalmente tenemos la respuesta?
- Ken Milne en The SGEM: SGEM #208 – No hace ninguna diferencia – Glucocorticoides para el tratamiento del shock séptico
- Rob Macsweeney en Critical Care Reviews (avance rápido hasta el minuto 1:01):
Publicación revisada por pares por: Anand Swaminathan (Twitter: @EMSwami )
La publicación El ensayo ADRENAL: esteroides en el shock séptico apareció por primera vez en REBEL EM - Blog de medicina de emergencia .
