

Antecedentes: ¿Podría Xuebijing (XBJ) catalizar un cambio de paradigma en el tratamiento de la sepsis? XBJ es un compuesto a base de hierbas utilizado en China para controlar diversos procesos inflamatorios e infecciosos en los últimos años, incluida la sepsis. 2-6 Es una preparación a base de hierbas que comprende una mezcla de cinco hierbas: Carthami Flos, Paeoniae Radix Rubra, Angelicae Sinensis Radix y Salviae Miltiorrhizae. 2,5,6 El profesor Jinda Wang lo desarrolló basándose en los principios de la medicina tradicional china para combatir las infecciones y la inflamación. 4 XBJ recibió la aprobación de la Administración de Alimentos y Medicamentos de China en 2004, 2 aunque la FDA de Estados Unidos no lo ha aprobado. Esta publicación evalúa el reciente ensayo “Eficacia de la inyección de Xuebijing en pacientes con sepsis (EXIT-SEP)”.
Artículo: Liu S, Yao C, Xie J, et al. Efecto de una inyección a base de hierbas sobre la mortalidad a 28 días en pacientes con sepsis: ensayo clínico aleatorizado EXIT-SEP. Médico Interno JAMA. 2023;e230780. PMID: 37126332
Pregunta clínica: En pacientes adultos diagnosticados con sepsis, ¿XBJ reduce la mortalidad a los 28 días cuando se agrega a la atención estándar en comparación con el placebo?
Que hicieron:
- Los investigadores realizaron un ensayo aleatorizado, doble ciego, controlado con placebo, multicéntrico y de grupos paralelos.
- Inscribieron consecutivamente a 1.817 pacientes de UCI de 45 sitios en toda China.
- Los pacientes fueron aleatorizados de forma 1:1.
- 911 pacientes fueron asignados al azar a la intervención y 906 al control.
- Se instruyó a los proveedores para que siguieran las pautas locales de manejo de la sepsis.
- Ensayo registrado en Clinicaltrial.gov: N CT03238742
- El Centro de Desarrollo proporcionó financiación para la Ciencia y Tecnología Médicas de la Comisión Nacional de Salud de la República Popular China.
Población:
Criterios de inclusión:
- Edad 18-75 años
- Puntuación SOFÁ 2-13
-
Ingresado en UCI con diagnóstico de sepsis 3.0,
- " Disfunción orgánica potencialmente mortal causada por una respuesta desregulada del huésped a la infección". 7 Clínicamente hablando, utilizaron un aumento de la puntuación SOFA de 2 o más puntos para indicar esto. Esto varía de la definición de 2001, que utilizaba criterios SIRS y se pensaba que se centraba demasiado en la inflamación. 7
Criterio de exclusión:
- Diagnosticado con sepsis durante más de 48 horas.
- Incapacidad para dar consentimiento
- Enfermedad primaria grave (tumores irresecables, enfermedades hematológicas, VIH)
- Disfunción hepática o renal grave
- Terapia con un inmunosupresor o trasplante de órgano reciente.
- Embarazo o lactancia
- Participación en otro ensayo clínico dentro de los 30 días.
Intervención:
- XBJ (100 ml) mezclado con 100 ml de solución salina normal (NS) cada 12 horas durante 5 días (volumen total de 200 cc).
Control:
- Placebo: 200 ml de NS cada 12 horas durante 5 días
Resultados:
Resultado primario:
- Mortalidad por todas las causas a los 28 días después de la aleatorización
Resultados secundarios:
- UCI y mortalidad hospitalaria
- Duración de la estancia en UCI y hospital
- Número de días libres de UCI a los 28 días
- Días acumulados sin ventilador a los 28 días
- Cambio en las puntuaciones de APACHE II y SOFA
Resultados de seguridad:
- Eventos adversos informados
Resultados:
Inscripción:
- Se examinaron 4692 participantes potenciales de 45 UCI entre los meses del 20 de octubre de 2017 al 20 de junio de 2019.
-
1.817 inscritos y aleatorizados
- 911 asignados al azar a la cohorte XBJ.
- 906 fueron asignados al azar a la cohorte Placebo.
-
67 no recibieron la intervención a la que fueron asignados aleatoriamente debido a lo siguiente:
- Muerte (10)
- Retirada del consentimiento (32)
- Descubrimiento posterior de los criterios de exclusión en el momento de la aleatorización (25)
- 1.325 (75,7%) completaron el período de tratamiento completo
- La puntuación SOFA inicial media fue de 7,1 en ambos grupos
- La puntuación media de APACHE II fue 12 en ambos grupos
- Casi la mitad de los pacientes tenían shock séptico al momento de la inscripción.
- El tiempo medio desde la identificación de la sepsis hasta la aleatorización fue de 1,4 días.
- Los 2 sitios de infección más comunes fueron el pulmón (44,8%) y el intraabdominal (32,1%).
- La mayoría de las infecciones fueron adquiridas en la comunidad (≈84%)
- Más de la mitad de los pacientes estaban con ventilación mecánica (≈53%)
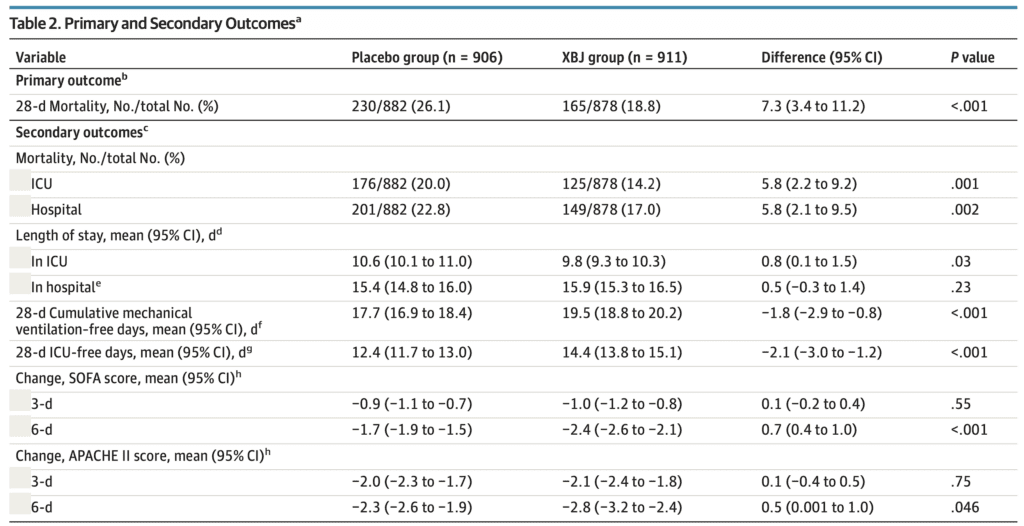
Resultados del resultado primario:
-
Tasa de mortalidad a 28 días:
- Placebo 26,1% (230/882) frente a XBJ 18,8% (165/878); P<0,001
- La diferencia de riesgo fue del 7,3% (IC del 95%, 3,4-11,2)
- 33 pacientes en el grupo de intervención y 24 en el grupo de placebo tenían un estado de mortalidad desconocido en el día 28 y se supuso que estaban vivos.
Resultados del resultado secundario:
-
Mortalidad en UCI:
- placebo 20,0% frente a XBJ 14,2%
- La diferencia de riesgo fue del 5,8 % (IC del 95 %, 2,2 a 9,2; P = 0,001)
-
Mortalidad hospitalaria:
- Placebo 22,8% frente a XBJ 17,0%
- La diferencia de riesgo fue del 5,8 % (IC del 95 %, 2,1 a 9,5; P = 0,002)
-
Días libres de UCI:
- Placebo 12,4% frente a XBJ 14,4%
- La diferencia de riesgo fue del –2,8 % (IC del 95 %: -3,0 a -1,2; p < 0,001)
-
Días sin ventilación mecánica acumulados de 28 días:
- Placebo 17,7% frente a XBJ 19,5%
- La diferencia de riesgo fue de –1,8 % (IC del 95 %: -2,9 a -0,8; p < 0,001)
Resultados de los resultados de seguridad:
-
Eventos adversos:
- 422 pacientes (24,1%) experimentaron al menos un evento adverso
- 200 pacientes (22,9%) en el grupo XBJ frente a 222 pacientes (25,3%) en el grupo placebo) dentro de los 28 días de seguimiento.
- No se suspendió ningún tratamiento debido a la toxicidad del fármaco.
-
Las transaminasas elevadas y la leucocitosis fueron más comunes en el grupo de XBJ
- ALT, 5,8 %, AST 4,4 % y WBC 4,1 %
- Distribuciones similares de eventos adversos entre XBJ y placebo sin eventos adversos graves relacionados con el fármaco informados.
Fortalezas:
- El diseño del ensayo multicéntrico, doble ciego, aleatorizado, controlado con placebo limita el sesgo y aumenta la validez externa.
- Los pacientes se inscribieron de forma consecutiva, lo que limita el sesgo de selección.
- El ensayo fue supervisado por un comité directivo ciego y una junta independiente de seguimiento de datos y seguridad.
- Los investigadores registraron el ensayo en Clinicaltrials.gov, aumentando la transparencia y la reproducibilidad.
- Los investigadores formularon una pregunta de investigación centrada en el paciente.
- El resultado primario estuvo orientado al paciente.
- El tamaño de la muestra fue grande.
- La tasa de mortalidad supuesta para el cálculo del poder estadístico fue precisa y el estudio tuvo el poder estadístico adecuado.
- La aleatorización y el ocultamiento utilizaron un sistema seguro basado en la web que limita el potencial de desenmascaramiento.
- Los datos demográficos, la gravedad de la enfermedad y las comorbilidades estuvieron bien equilibrados entre los grupos y los grupos de intervención y control tienen el mismo pronóstico.
-
Los investigadores realizaron un análisis por intención de tratar que analiza a los pacientes en los grupos que les asignaron, independientemente de que siguieran o no el protocolo del estudio.
- Esto refleja una práctica clínica del mundo real que mantiene la aleatorización y limita el sesgo.
-
Los investigadores realizaron múltiples análisis de sensibilidad que confirmaron los resultados principales, aumentando aún más la credibilidad y solidez de los datos.
- Análisis del peor escenario posible
- Análisis del punto de inflexión
Limitaciones:
- La composición de XBJ complica la determinación de los compuestos específicos responsables de los efectos observados.
- La inscripción de pacientes exclusivamente de un solo país (China) restringe la aplicabilidad de los hallazgos a poblaciones globales diversas.
- La inclusión limitada del estudio de pacientes gravemente enfermos (puntuación APACHE >25, disfunción renal o hepática grave) afecta su relevancia para los pacientes más enfermos con un mayor riesgo de enfermedades comórbidas.
- Las razones más comunes de exclusión incluyeron disfunción hepática y renal grave, enfermedad primaria grave y diagnóstico de sepsis ≥48 horas. Esto limita la generalización a pacientes con disfunción multiorgánica, diagnósticos terminales y presentaciones tardías.
- El estudio tuvo el poder para detectar diferencias en los resultados secundarios, pero esto debe interpretarse con cautela ya que hubo diez resultados secundarios sin ajustes para comparaciones múltiples (es decir, generación de hipótesis).
- Muchos de los resultados secundarios se cambiaron mucho después de que se adquiriera la mayoría de los datos.
- Casi dos tercios de la población inscrita eran hombres, lo que limita la generalización.
- Realizar el estudio únicamente en la UCI limita su transferibilidad a otros entornos de tratamiento, como el servicio de urgencias.
- La distribución de los pacientes inscritos en cada centro sigue sin especificarse, lo que podría comprometer la generalización de los datos si unos pocos centros contribuyeran con un número sustancial de participantes.
- Existía la posibilidad de desenmascaramiento debido a las diferencias en la apariencia de los fármacos, junto con el conocimiento de las enfermeras del estudio, y su participación en la atención al paciente sigue sin estar clara.
- La administración de antibióticos antes de la aleatorización introduce incertidumbre sobre su impacto en los datos recopilados.
- Una mayor proporción de casos de seguimiento perdidos dentro del grupo XBJ introduce un sesgo.
- El predominio de infecciones pulmonares e intraabdominales (que constituyen casi el 80% de los casos) limita la aplicabilidad más amplia de XBJ a infecciones de otras fuentes.
- La falta de datos de seguimiento a largo plazo dificulta la comprensión de los resultados del tratamiento prolongado.
- XBJ, una preparación a base de hierbas sin la aprobación de la FDA, puede plantear desafíos en países que no están familiarizados con la medicina alternativa/complementaria.
Discusión:
Dentro de los números:
- El número necesario a tratar (NNT) es un concepto fundamental en la investigación clínica. 8 Ayuda a traducir el impacto del tratamiento en una estadística más comprensible y clínicamente relevante. 8 El NNT para XBJ en este artículo es 13,7, lo que indica que, en promedio, alrededor de 14 pacientes con sepsis necesitarían ser tratados con XBJ para prevenir una muerte en 28 días.
- El índice de fragilidad mide la solidez de los resultados de un ensayo clínico, especialmente su importancia estadística para el resultado primario. Mide cómo los cambios en los resultados en los grupos de tratamiento y control podrían alterar los hallazgos del estudio. Un índice bajo indica conclusiones frágiles, fácilmente revertidas por unos pocos acontecimientos. Un índice alto refleja resultados sólidos, resistentes a fluctuaciones de eventos menores. El índice de fragilidad de 29 de este artículo indica que se necesitan cambios en los eventos de resultado de 29 pacientes para alterar la significación estadística de los resultados del estudio.
- Treinta y tres pacientes se perdieron durante el seguimiento y los investigadores realizaron múltiples análisis de sensibilidad en estos pacientes. El análisis de sensibilidad evalúa exhaustivamente los resultados del estudio al tiempo que considera varios escenarios y factores que podrían influir en los resultados. Al alterar sistemáticamente ciertas variables o suposiciones, los investigadores pueden evaluar la solidez y confiabilidad de sus hallazgos. El análisis de sensibilidad de este artículo confirmó los hallazgos iniciales y demostró que las conclusiones del estudio se mantienen incluso bajo diversas condiciones, lo que refuerza la confiabilidad y credibilidad de los resultados de la investigación. Para cambiar el resultado del estudio, casi los 33 pacientes perdidos durante el seguimiento tendrían que cumplir el resultado primario dentro del grupo experimental.
¿Perfectamente plausible?:
- Los datos son apasionantes y dignos de mención. Sin embargo, es fundamental recordar que los investigadores excluyeron a muchos pacientes muy enfermos. Por lo tanto, la población estudiada se encontraba relativamente sana al iniciar el estudio. Además, los pacientes ya comenzaron el tratamiento con antibióticos antes de ser asignados aleatoriamente a recibir XBJ o placebo, lo que puede sobreestimar o alterar los hallazgos. Además, XBJ contiene muchos compuestos cuyos mecanismos exactos no están claros. Si bien es posible que algunos de sus componentes sean beneficiosos, es poco probable que todos los componentes sean activos contra la sepsis. Los hallazgos recuerdan a otras terapias recientes con vitamina C para la sepsis, que finalmente demostraron ser ineficaces en estudios de validación de seguimiento.
Xuebijing y la FDA
- Aunque el Xuebijing figura como un suplemento a base de hierbas utilizado para tratar una enfermedad específica, una formulación intravenosa probablemente estaría sujeta a los requisitos de aprobación exactos de cualquier medicamento nuevo. 9 Específicamente, debe haber una solicitud de licencia con dos estudios que demuestren que los beneficios del medicamento superan los riesgos. 9 Ocasionalmente, la FDA aprobará un medicamento basándose en un único estudio de alta calidad que cubra una amplia gama de pacientes con beneficios claros. 9 Si bien hay un beneficio significativo y pocos efectos adversos discutidos en este estudio, no demuestra suficiente validez externa para ser aplicado a pacientes en el servicio de urgencias. Como tal, para que la FDA considere la aprobación de XBJ, se requeriría un estudio adicional en una amplia gama de pacientes, preferiblemente en una población estadounidense o internacional más representativa del paciente séptico en los Estados Unidos.
Conclusiones de los autores: "En este ensayo clínico aleatorizado entre pacientes con sepsis, la administración de XBJ redujo la mortalidad a los 28 días en comparación con el placebo".
Conclusión clínica:
XBJ muestra potencial para mejorar las tasas de supervivencia de los pacientes con sepsis. Sin embargo, su composición parece ser una variedad aleatoria de hierbas con dosis variables. Si bien el estudio es prometedor, se debe establecer y verificar una formulación más precisa en ensayos adicionales antes de que pueda integrarse en la práctica clínica.
Más sobre este tema:
- First10EM: Finalmente, una cura para la sepsis: hierbas
- REBEL EM: Sepsis 3.0 Definiciones
- REBEL EM: Azul de metileno para la sepsis
- REBEL EM: VITAMINAS para la sepsis
Referencias:
- Liu S, Yao C, Xie J, et al. Efecto de una inyección a base de hierbas sobre la mortalidad a 28 días en pacientes con sepsis: ensayo clínico aleatorizado EXIT-SEP. Médico Interno JAMA. 2023;e230780. PMID: 37126332
- Song Y, Yao C, Yao Y, Han H, Zhao X, Yu K, Liu L, Xu Y, Liu Z, Zhou Q, Wang Y, Ma Z, Zheng Y, Wu D, Tang Z, Zhang M, Pan S , Chai Y, Song Y, Zhang J, Pan L, Liu Y, Yu H, Yu X, Zhang H, Wang X, Du Z, Wan X, Tang Y, Tian Y, Zhu Y, Wang H, Yan X, Liu Z, Zhang B, Zhong N, Shang H, Bai C. Inyección de XueBiJing versus placebo para pacientes críticamente enfermos con neumonía grave adquirida en la comunidad: un ensayo controlado aleatorio. Medicina de cuidados críticos. 2019 septiembre;47(9):e735-e743. PMID: 31162191
- Zheng J, Xiang X, Xiao B, Li H, Gong X, Yao S, Yuan T. Xuebijing combinado con ulinastation beneficia a los pacientes con sepsis: un metanálisis. Soy J Emerg Med. Marzo de 2018;36(3):480-487. doi: 10.1016/j.ajem.2017.12.007. Publicación electrónica del 16 de enero de 2018. PMID: 29373169.
- Han D, Wang R, Yu Y, Sun M, Teschke R, Romeiro FG, Mancuso A, Song T, Peng Z, Han B, Zhou X, Bao W, Li Q, Zheng K, Li Y, Bai Z, Guo X , Qi X. Inyección de Xuebijing combinada con antibióticos para el tratamiento de la peritonitis bacteriana espontánea en la cirrosis hepática: un metaanálisis. Complemento basado en Evid Alternat Med. 19 de marzo de 2018; 2018: 2989846. PMID: 29743922
- Chen H, Bai Z, Li H, Wu Y, Yao H, Wang L, Lin H, Tong Z, Teschke R, Qi X. Eficacia de la inyección de Xuebijing para la pancreatitis aguda: una revisión sistemática y un metanálisis de ensayos controlados aleatorios. Complemento basado en Evid Alternat Med. 26 de abril de 2021; 2021:6621368. PMID: 34221082
- Lv J, Guo X, Zhao H, Zhou G, An Y. La administración de Xuebijing alivia la inflamación endotelial pulmonar y la desregulación de la coagulación en la fase temprana de la sepsis en ratas. J Clin Med. 11 de noviembre de 2022; 11 (22): 6696. PMID: 36431172
- Singer M, Deutschman CS, Seymour CW, Shankar-Hari M, Annane D, Bauer M, Bellomo R, Bernard GR, Chiche JD, Coopersmith CM, Hotchkiss RS, Levy MM, Marshall JC, Martin GS, Opal SM, Rubenfeld GD, van der Poll T, Vincent JL, Angus DC. Las definiciones del tercer consenso internacional para sepsis y shock séptico (Sepsis-3). JAMA. 23 de febrero de 2016; 315 (8): 801-10. PMID: 26903338
Publicación invitada por:

Lynnsey Moss, MD
PGY-3, Jefe de Residentes de Medicina de Emergencia
Hospital Vassar Brothers, Poughkeepsie, Nueva York
Correo electrónico: lynnsey.moss@nuvancehealth.org

Marco Propersi, DO FAAEM
Vicepresidente de Medicina de Emergencia
Director asistente del programa de residencia en medicina de emergencia
Hospital Vassar Brothers, Poughkeepsie, Nueva York
Gorjeo: @marco_propersi
Revisión posterior por pares por: Salim R. Rezaie, MD (Twitter: @srrezaie )
El post Una esperanza a base de hierbas: ¿Es XBJ un punto de inflexión en el tratamiento de la sepsis? apareció por primera vez en REBEL EM - Blog de Medicina de Emergencia .
