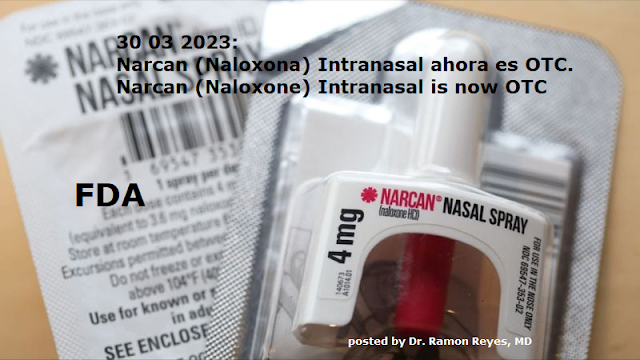
La FDA aprueba el primer aerosol nasal de naloxona de venta libre
La agencia continúa tomando medidas críticas para reducir las muertes por sobredosis de drogas provocadas principalmente por opioides ilícitos.
29 de marzo de 2023
Inglés
Hoy, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA, por sus siglas en inglés) aprobó Narcan, un aerosol nasal de clorhidrato de naloxona de 4 miligramos (mg), para uso de venta libre, sin receta médica; es el primer producto de naloxona aprobado para su uso sin prescripción. La naloxona es un medicamento que revierte rápidamente los efectos de una sobredosis de opioides y es el tratamiento acostumbrado para la sobredosis de opioides. La acción de hoy cimienta el camino para que este medicamento que salva vidas revierta una sobredosis de opioides y se venda directamente a los consumidores en lugares como farmacias, tiendas de conveniencia, supermercados y gasolinaras, así como en línea.
El plazo para la disponibilidad y el precio de este producto de venta libre lo determina el fabricante. La FDA trabajará con todas las partes interesadas para ayudar a facilitar la disponibilidad constante de productos de aerosol nasal de naloxona durante el tiempo necesario para efectuar el cambio de que Narcan pase a ser un medicamento que requiere receta médica a uno de venta libre, lo que puede tardar meses. Otras formulaciones y dosis de naloxona permanecerán disponibles solo con receta médica.
La sobredosis de drogas persiste como un importante problema de salud pública en los Estados Unidos, con más de 101,750 sobredosis fatales reportadas que ocurrieron en el período de 12 meses que finalizó en octubre de 2022, causadas principalmente por opioides sintéticos como el fentanilo ilícito.
“La FDA mantiene su compromiso de ocuparse de las complejidades cambiantes de la crisis de sobredosis. Como parte de este trabajo, la agencia ha utilizado su autoridad normativa para facilitar un mayor acceso a la naloxona al alentar el desarrollo y la aprobación de un producto de naloxona de venta libre para responder a la urgente necesidad de salud pública”, afirmó el comisionado. de la FDA, el doctor Robert M. Califf. “La aprobación de hoy del aerosol nasal de naloxona de venta libre ayudará a mejorar el acceso a la naloxona, aumentará la cantidad de lugares donde está disponible y ayudará a reducir las muertes por sobredosis de opioides en todo el país. Animamos al fabricante a que priorice la accesibilidad al producto, haciendo disponible lo antes posible ya un precio accesible”.
El aerosol nasal Narcan fue aprobado por primera vez por la FDA en 2015 como medicamento recetado. De acuerdo con un proceso para cambiar el estado de un medicamento de venta con receta a venta sin receta, el fabricante proporcionó datos que demuestran que el medicamento es seguro y eficaz para su uso según las indicaciones de la etiqueta propuesta. El fabricante también demostró que los consumidores pueden entender cómo usar el medicamento de manera segura y eficaz sin la supervisión de un profesional de la salud. La solicitud para aprobar el aerosol nasal Narcan para uso de venta libre recibió el estado de revisión prioritaria y fue objeto de una reunión del comité asesor en febrero de 2023, donde los miembros del comité votaron unánimemente para recomendar que se aprobara para su comercialización sin receta. .
La aprobación del aerosol nasal Narcan de venta libre requerirá un cambio en la etiqueta de los productos genéricos de aerosol nasal de naloxona de 4 mg actualmente aprobados que dependen de Narcan como su producto farmacéutico de referencia. Los fabricantes de estos productos deberán presentar un complemento a sus solicitudes para cambiar efectivamente sus productos al estado de venta libre. La aprobación también puede afectar el estado de otras marcas de aerosol nasal de naloxona de 4 mg o inferior, pero las determinaciones se realizarán caso por caso y la FDA puede comunicarse con otras empresas según sea necesario.
El uso del aerosol nasal Narcan en personas que son dependientes de los opioides puede provocar una abstinencia grave de los opioides caracterizada por dolores corporales, diarrea, aumento de la frecuencia cardíaca (taquicardia), fiebre, moqueo, estornudos, piel de gallina, sudoración, bostezos, náuseas o vómitos, nerviosismo, inquietud o irritabilidad, escalofríos o temblores, calambres abdominales, debilidad y aumento de la presión arterial.
“La naloxona es una herramienta clave para abordar las sobredosis de opioides y la aprobación de hoy destaca los amplios esfuerzos que la agencia ha realizado para combatir la crisis de sobredosis”, expresó la doctora Patrizia Cavazzoni, directora del Centro de Evaluación e Investigación de Medicamentos de la FDA. “La FDA trabaja con nuestros colaboradores federales a fin de garantizar el acceso continuo a naloxona en todas sus presentaciones durante la transición de este producto del estado de venta con receta al estado de venta sin receta a de venta libre. Además, trabajaremos con cualquier patrocinador que busque comercializar un producto de naloxona sin receta, incluso a través de un cambio de venta con receta a de venta libre, y exhortaremos a los fabricantes a comunicarse con la agencia lo antes posible para iniciar conversaciones”.
La FDA ha adoptado una serie de medidas para ayudar a facilitar el acceso a los productos de naloxona. En noviembre de 2022, la agencia anunció su evaluación preliminar de que ciertos productos de naloxona, como el que finalmente se aprobó hoy, tienen el potencial de ser seguros y eficaces para su uso sin receta y animó a los patrocinadores a presentar solicitudes. para la aprobación de productos de naloxona de venta libre. La agencia anunció previamente en 2019 que había diseñado, probado y validado un modelo de etiqueta de información del medicamento (DFL, por sus siglas en inglés) de naloxona con pictogramas fáciles de entender sobre cómo usar el medicamento para alentar a los fabricantes a buscar la aprobación de productos de naloxona de venta libre. El modelo DFL se utiliza para respaldar la solicitud aprobada junto con los resultados de un estudio de validación de factores humanos de uso simulado diseñado para evaluar si todos los componentes del producto con los que un usuario interactuaría podrían usarse de manera segura y eficaz según lo previsto. .
A través del Marco de prevención de sobredosis de la FDA, la agencia sigue enfocada en responder a todas las facetas del consumo de sustancias, el consumo indebido, los trastornos por el consumo de sustancias, las sobredosis y la muerte en los Estados Unidos. Las prioridades del marco incluyen: apoyar la prevención primaria al eliminar la exposición inicial innecesaria a medicamentos recetados y la prescripción prolongada inapropiada; fomentar la reducción de daños a través de la innovación y la educación; avanzar en el desarrollo de tratamientos basados en evidencia para los trastornos por consumo de sustancias; y proteger al público de medicamentos no aprobados, desviados o falsificados que presenten riesgos de sobredosis.
La FDA otorgó la aprobación de venta libre de Narcan a Emergent BioSolutions.
La FDA aprueba el primer aerosol nasal de naloxona de venta libre
La agencia continúa tomando medidas críticas para reducir las muertes por sobredosis de drogas provocadas principalmente por opioides ilícitos
Leer en FDA en inglés
Hoy, la Administración de Alimentos y Medicamentos de EE. UU. aprobó Narcan, 4 miligramos (mg) de hidrocloruro de naloxona en aerosol nasal para uso sin receta, sin receta, el primer producto de naloxona aprobado para su uso sin receta. La naloxona es un medicamento que revierte rápidamente los efectos de una sobredosis de opioides y es el tratamiento estándar para la sobredosis de opioides. La acción de hoy allana el camino para que el medicamento que salva vidas revierta una sobredosis de opioides se venda directamente a los consumidores en lugares como farmacias, tiendas de conveniencia, supermercados y gasolineras, así como en línea.
El cronograma de disponibilidad y el precio de este producto de venta libre lo determina el fabricante. La FDA trabajará con todas las partes interesadas para ayudar a facilitar la disponibilidad continua de productos en aerosol nasal de naloxona durante el tiempo necesario para implementar el cambio de Narcan de prescripción a venta libre, lo que puede llevar meses. Otras formulaciones y dosis de naloxona seguirán estando disponibles únicamente con receta médica.
La sobredosis de drogas persiste como un importante problema de salud pública en los Estados Unidos, con más de 101,750 sobredosis fatales reportadas en el período de 12 meses que finalizó en octubre de 2022, impulsadas principalmente por opioides sintéticos como el fentanilo ilícito.
“La FDA sigue comprometida a abordar las complejidades cambiantes de la crisis de sobredosis. Como parte de este trabajo, la agencia ha utilizado su autoridad regulatoria para facilitar un mayor acceso a la naloxona fomentando el desarrollo y la aprobación de un producto de naloxona de venta libre para abordar la grave necesidad de salud pública”, dijo el comisionado de la FDA, Robert M. Califf. , MD “La aprobación de hoy del aerosol nasal de naloxona de venta libre ayudará a mejorar el acceso a la naloxona, aumentará la cantidad de lugares donde está disponible y ayudará a reducir las muertes por sobredosis de opioides en todo el país. Alentamos al fabricante a que haga de la accesibilidad del producto una prioridad poniéndolo a disposición lo antes posible y a un precio asequible”.
El aerosol nasal Narcan fue aprobado por primera vez por la FDA en 2015 como medicamento recetado. De acuerdo con un proceso para cambiar el estado de un medicamento de recetado a sin receta, el fabricante proporcionó datos que demuestran que el medicamento es seguro y eficaz para su uso según lo indicado en la etiqueta propuesta. El fabricante también demostró que los consumidores pueden entender cómo utilizar el medicamento de forma segura y eficaz sin la supervisión de un profesional sanitario. A la solicitud para aprobar el aerosol nasal Narcan para uso sin receta se le otorgó el estado de revisión prioritaria y fue objeto de una reunión del comité asesor en febrero de 2023, donde los miembros del comité votaron por unanimidad para recomendar que se aprobara su comercialización sin receta.
La aprobación del aerosol nasal Narcan de venta libre requerirá un cambio en el etiquetado de los productos en aerosol nasal genéricos de naloxona de 4 mg actualmente aprobados que dependen de Narcan como su medicamento de referencia. Los fabricantes de estos productos deberán presentar un suplemento a sus solicitudes para cambiar efectivamente sus productos al estado OTC. La aprobación también puede afectar el estado de otros productos de marca en aerosol nasal de naloxona de 4 mg o menos, pero las determinaciones se harán caso por caso y la FDA puede comunicarse con otras empresas según sea necesario.
El uso de Narcan en aerosol nasal en personas dependientes de opioides puede provocar una abstinencia grave de opioides caracterizada por dolores corporales, diarrea, aumento del ritmo cardíaco (taquicardia), fiebre, secreción nasal, estornudos, piel de gallina, sudoración, bostezos, náuseas o vómitos. nerviosismo, inquietud o irritabilidad, escalofríos o temblores, calambres abdominales, debilidad y aumento de la presión arterial.
"La naloxona es una herramienta fundamental para abordar las sobredosis de opioides y la aprobación de hoy subraya los amplios esfuerzos que la agencia ha realizado para combatir la crisis de sobredosis", dijo Patrizia Cavazzoni, MD, directora del Centro de Evaluación e Investigación de Medicamentos de la FDA. “La FDA está trabajando con nuestros socios federales para ayudar a garantizar el acceso continuo a todas las formas de naloxona durante la transición de este producto del estado con receta al estado sin receta/OTC. Además, trabajaremos con cualquier patrocinador que busque comercializar un producto de naloxona sin receta, incluso mediante un cambio de receta a venta libre, y alentaremos a los fabricantes a que se comuniquen con la agencia lo antes posible para iniciar conversaciones”.
La FDA ha tomado una serie de medidas para ayudar a facilitar el acceso a los productos de naloxona. En noviembre de 2022, la agencia anunció su evaluación preliminar de que ciertos productos de naloxona, como el que finalmente se aprobó hoy, tienen el potencial de ser seguros y eficaces para uso sin receta y alentó a los patrocinadores a presentar solicitudes para la aprobación de productos de naloxona de venta libre. . La agencia anunció previamente en 2019 que había diseñado, probado y validado un modelo de etiqueta de información sobre el medicamento (DFL) de naloxona con pictogramas fáciles de entender sobre cómo usar el medicamento para alentar a los fabricantes a buscar la aprobación de productos de naloxona de venta libre. El modelo DFL se utilizó para respaldar la aplicación aprobada junto con los resultados de un estudio de validación de factores humanos de uso simulado diseñado para evaluar si todos los componentes del producto con los que interactuaría un usuario podrían usarse de manera segura y efectiva según lo previsto.
A través del Marco de Prevención de Sobredosis de la FDA, la agencia sigue enfocada en responder a todas las facetas del uso de sustancias, el uso indebido, los trastornos por uso de sustancias, las sobredosis y la muerte en los EE. UU. Las prioridades del marco incluyen: apoyar la prevención primaria mediante la eliminación de la exposición inicial innecesaria a medicamentos recetados y la exposición prolongada inapropiada prescribir; fomentar la reducción de daños a través de la innovación y la educación; promover el desarrollo de tratamientos basados en evidencia para los trastornos por uso de sustancias; y proteger al público de medicamentos no aprobados, desviados o falsificados que presenten riesgos de sobredosis.
La FDA otorgó la aprobación de venta libre de Narcan a Emergent BioSolutions. https://www.fda.gov/news-events/press-announcements/fda-approves-first-over-counter-naloxone-nasal-spray
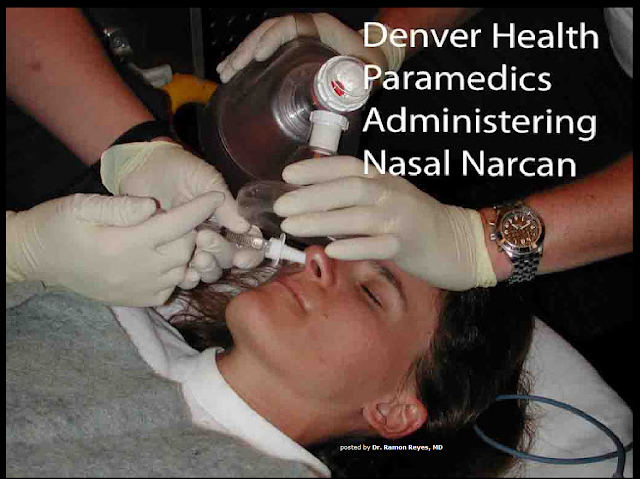
Estudio: EMT de Nueva York administran dosis intranasales de Narcan
Información de EMSWORLD
Hasta ahora, el antídoto contra la sobredosis de medicamentos sólo lo administraban proveedores de ELA.
Por favor comparta nuestras REDES SOCIALES @DrRamonReyesMD, así podremos llegar a más personas y estos se beneficiarán de la disponibilidad de estos documentos, pdf, e-book, gratuitos y legales.
Grupo Biblioteca/PDFs gratis en Facebook
https://www.facebook.com/groups/PDFgratisMedicina #DrRamonReyesMD
https://www.facebook.com/DrRamonReyesMD
https://www.instagram.com/drramonreyesmd/
https://www.pinterest.es/DrRamonReyesMD/
Gorjeo
https://twitter.com/eeiispain
Blog
http://emssolutionsint.blogspot.com/2016/12/dr-ramon-reyes-diaz-md-emt-t-dmo.html
TELEGRAMA
Grupo https://t.me/joinchat/GRsTvEHYjNLP8yc6gPXQ9Q