
 Antecedentes: El TXA es un derivado de lisina sintético que se une al sitio de lisina en el plasminógeno e inhibe la fibrinólisis. TXA no es un medicamento nuevo. Estudios de finales de los años 1960 y principios de los 1970 han demostrado una reducción del sangrado y de la necesidad de transfusiones en muchos entornos médicos y quirúrgicos. Avance rápido hasta el día de hoy y estamos encontrando todo tipo de usos para TXA además de traumatismos, incluida la hemorragia posparto, epistaxis, hemoptisis, hemorragia gastrointestinal y muchos más.
Antecedentes: El TXA es un derivado de lisina sintético que se une al sitio de lisina en el plasminógeno e inhibe la fibrinólisis. TXA no es un medicamento nuevo. Estudios de finales de los años 1960 y principios de los 1970 han demostrado una reducción del sangrado y de la necesidad de transfusiones en muchos entornos médicos y quirúrgicos. Avance rápido hasta el día de hoy y estamos encontrando todo tipo de usos para TXA además de traumatismos, incluida la hemorragia posparto, epistaxis, hemoptisis, hemorragia gastrointestinal y muchos más.
Trauma
MATTERs (Estudio sobre la aplicación militar del ácido tranexámico en la reanimación de emergencias por traumatismos) [1]
Que hicieron:
- Este fue un estudio observacional retrospectivo, de un solo centro, en un hospital regional de Afganistán, que comparó ATX versus ningún ATX en pacientes que recibieron al menos 1 unidad de glóbulos rojos. Los autores del estudio también evaluaron a pacientes que recibieron transfusión masiva (≥10 unidades de glóbulos rojos). El régimen de dosificación estándar para TXA fue 1 g IV con dosis repetidas según lo determine el médico tratante.
Resultados:
- Los resultados principales (primarios) fueron la mortalidad a las 24 horas, la mortalidad a las 48 horas y la mortalidad a los 30 días. Los resultados secundarios destacados fueron los requisitos de transfusión y la tasa de complicaciones tromboembólicas.
Inclusión:
- Pacientes traumatizados consecutivos, con lesiones relacionadas con el combate, que recibieron al menos 1 unidad de glóbulos rojos dentro de las 24 horas posteriores al ingreso.
Resultados:
- El ensayo incluyó a 896 pacientes con lesiones de combate, de los cuales 293 (32,7%) recibieron TXA dentro de la primera hora posterior a la lesión.
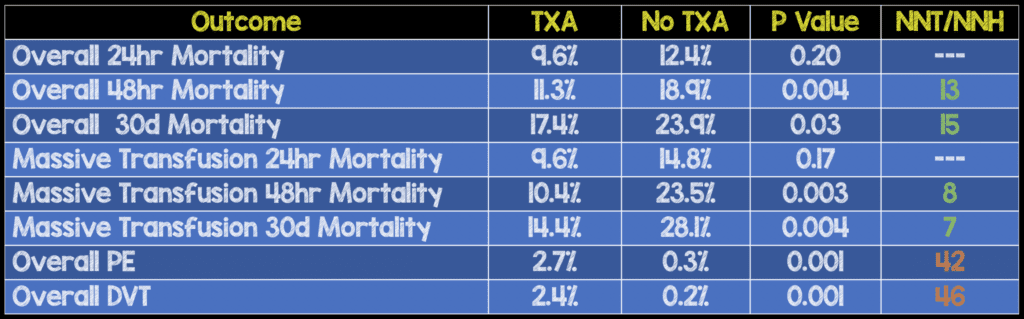
- ATX asociado independientemente con la supervivencia: OR 7,228; IC 95% 3,016 – 17,322
- NO HAY MUERTES por TEV
Fortalezas:
- Primer estudio que informa sobre las lesiones en tiempos de guerra, que pueden diferir de las lesiones civiles (es decir, traumatismos penetrantes frente a traumatismos contundentes)
- Se incluyeron pacientes consecutivos, lo que significa que todos los pacientes que cumplieron con los criterios de inclusión se incluyeron en este estudio controlando el sesgo de muestreo (es decir, no se omitieron pacientes que puedan ocurrir en el muestreo de conveniencia)
Limitaciones:
- Las pautas de práctica clínica, incluido el uso de TXA, no se introdujeron hasta la última parte del período del estudio, lo que significa que puede haber habido ligeras variaciones en las indicaciones de uso y dosificación del medicamento durante la mayor parte del estudio.
- Debido al pequeño número de eventos de TEV, no está claro si el aumento de la tasa de TEV con el ATX se debe al ATX en sí o a la carga de la lesión.
- Los autores no pudieron determinar la causa exacta ni el momento de la muerte en los pacientes que fallecieron. Por lo tanto, se incluyen en el estudio algunos pacientes que murieron temprano durante el curso de su reanimación, pero muchos de estos pacientes pueden no haber sido afectados por ninguna intervención terapéutica.
Discusión:
- Se trataba de una cohorte bastante joven de pacientes con una edad promedio de aproximadamente 24 años y la mayoría de las lesiones fueron traumatismos penetrantes, no traumatismos contundentes (es decir, casi el 100% de los participantes incluidos). Los pacientes en el grupo de TXA, en general, estaban más enfermos con puntuaciones medias más altas de gravedad de la lesión (25,2 frente a 22,5), puntuación GCS ≤8 (63,3% frente a 35,6%), PAS ≤90 mmhg (22,8% frente a 13,8%) y tiempo medio. en el quirófano (170 min frente a 115 min), lo que significa que este estudio probablemente subestimó los efectos beneficiosos del ATX. La tasa más alta de TEV en el grupo de ATX debe tomarse con cautela, ya que estos pacientes también tuvieron una mayor carga de lesiones, que también pueden estar asociadas con eventos trombóticos.
Conclusión del autor: “El uso de TXA con reanimación basada en componentes sanguíneos después de una lesión de combate da como resultado mejores medidas de coagulopatía y supervivencia, un beneficio que es más prominente en pacientes que requieren transfusión masiva. El tratamiento con TXA debe implementarse en la práctica clínica como parte de la estrategia de reanimación después de lesiones y hemorragias graves en tiempos de guerra”.
Punto clínico para recordar: en pacientes con lesiones penetrantes que requirieron transfusiones de sangre dentro de la hora siguiente a la presentación, el uso de TXA redujo la mortalidad general. Este efecto fue aún más pronunciado en pacientes que requirieron transfusiones masivas (≥10 glóbulos rojos). No queda claro en este estudio si el aumento de eventos de TEV en el grupo de ATX se debe al ATX en sí o a la mayor carga de lesión. No hubo muertes debido a TEV en este ensayo.
Aleatorización clínica de un antifibrinolítico en hemorragia significativa 2 (CRASH – 2) [2]
Que hicieron:
- Este fue un ensayo multicéntrico, doble ciego, aleatorizado y controlado con placebo que incluyó 274 hospitales en 40 países, incluidos 20.211 pacientes adultos traumatizados con o en riesgo de hemorragia significativa, aleatorizados dentro de las 8 horas posteriores a la lesión a cualquiera de los ATX (dosis de carga de 1 g durante 10 minutos). , luego infusión de 1 g durante 8 horas) o placebo (solución salina normal al 0,9%).
Resultados:
- El resultado primario fue la mortalidad por todas las causas dentro de las 4 semanas posteriores a la lesión. Los resultados secundarios incluyeron: eventos vasculares oclusivos (IAM, accidente cerebrovascular, EP y TVP), intervención quirúrgica, recepción de transfusión de sangre y unidades de hemoderivados transfundidos.
Inclusión:
- Pacientes traumatizados adultos
- Hemorragia significativa (PAS <90 mmHg o FC >110 LPM o ambas)
- En riesgo de hemorragia significativa.
- Dentro de las 8 horas posteriores a la lesión
Resultados:
- 20.211 pacientes fueron asignados aleatoriamente a TXA (10.060 pacientes analizados) o placebo (10.067 pacientes analizados).
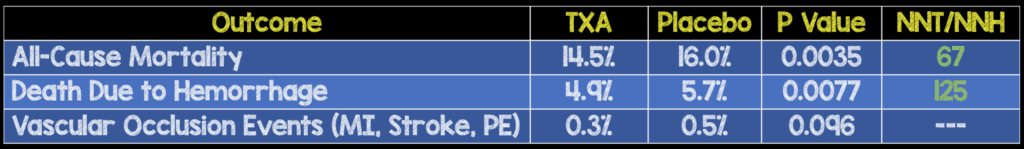
- No hay diferencias en el número de hemoderivados transfundidos ni en la necesidad de cirugía
- Los pacientes con PAS <75 mmHg tuvieron el mayor beneficio con el ATX (RR 0,87; IC del 95 %: 0,76 – 0,99)
Fortalezas:
- Todos los participantes e investigadores estaban cegados a la asignación del tratamiento, eliminando sesgos conscientes e inconscientes que podrían afectar el ensayo.
- Todos los hallazgos se registraron como intención de tratar, que se basa en la asignación de tratamiento inicial y no en si el paciente realmente recibió el tratamiento o no.
- El plan de análisis estadístico se envió al comité de ética y a las agencias reguladoras antes de revelar los resultados.
- Los financiadores del estudio no tuvieron ningún papel en el diseño del estudio, la recopilación de datos, el análisis de los datos, la interpretación de los datos o la redacción del informe, lo que garantiza que no haya influencias de las grandes farmacéuticas en los resultados.
- Los criterios de inclusión para este ensayo no dependieron de los resultados de las pruebas de laboratorio, lo que hace que los resultados de este estudio sean aplicables en un entorno del mundo real.
Limitaciones:
- El número de pacientes en la categoría temprana (≤1 hora) fue bajo y, por lo tanto, las estimaciones de subgrupos en este grupo no fueron precisas.
- Al igual que en el ensayo MATTERs, el número de eventos vasooclusivos fue tan pequeño que no se puede excluir la posibilidad de que el ATX aumente estos eventos.
Discusión:
- Casi 2/3 de los pacientes fueron asignados al azar ≤3 horas después de la lesión y tuvieron un traumatismo cerrado, no un traumatismo penetrante. Además, en comparación con el ensayo MATTERs, esta población de pacientes tampoco parecía estar tan enferma: >2/3 de los pacientes tenían una PAS ≥90 mmHg y una GCS de 13 a 15. Finalmente, el número de pacientes con lesión cerebral traumática fue muy pequeño en este estudio (270 pacientes), lo que limita cualquier conclusión en esta población de pacientes.
Conclusión del autor: “El ácido tranexámico redujo de forma segura el riesgo de muerte en pacientes con traumatismos hemorrágicos en este estudio. Sobre la base de estos resultados, se debe considerar el uso del ácido tranexámico en pacientes con traumatismos hemorrágicos”.
Punto clínico para recordar: el uso de TXA en pacientes traumatizados con “sangrado significativo” reduce la mortalidad por todas las causas sin un aumento de los eventos tromboembólicos. Este efecto parece ser mayor en el subconjunto de pacientes con shock grave (PAS ≤70 mmHg) y cuando se administra ≤3 horas desde el momento de la lesión (este punto final se confirmó en el metanálisis de los ensayos CRASH-2 y WOMAN [6 ].
Conclusión clínica: en pacientes traumatizados que requieren productos sanguíneos (es decir, protocolo de transfusión masiva), el uso de TXA como un bolo de 1 g administrado durante 10 minutos, seguido de 1 g durante 8 horas, en ≤ 3 horas desde el momento de la lesión, reduce todas las causas. mortalidad sin un aumento de eventos tromboembólicos.
TCE
Metaanálisis de TXA para lesiones cerebrales traumáticas [3]
Que hicieron:
- Este fue un metanálisis y una revisión sistemática de ECA o cuasialeatorios que compararon TXA versus placebo en pacientes con TBI y evaluaron sus resultados.
Resultados:
- Los principales resultados de interés incluyeron mortalidad, función neurológica, expansión del hematoma y efectos adversos, todos los cuales son resultados orientados al paciente.
Resultados:
- Dos ECA de alta calidad con 510 pacientes con TCE cumplieron los criterios de inclusión para esta revisión. Los efectos de los TXA sobre los resultados mencionados anteriormente fueron los siguientes:

- No se asociaron efectos adversos graves con el TXA.
Fortalezas:
- Ambos ensayos incluidos en este metanálisis tuvieron evidencia de alta calidad (es decir, doble ciego, análisis por intención de tratar, aleatorizado y seguimiento >92%).
Limitaciones:
- La mayor limitación de este metanálisis y revisión sistemática es el hecho de que sólo se pudieron encontrar 2 ECA y que ninguno de ellos tenía el poder estadístico adecuado para detectar resultados clínicos. En segundo lugar, los pacientes inscritos en CRASH-2 tenían lesiones extracraneales importantes y no solo TCE aislados. Por lo tanto, es factible que la tendencia hacia un beneficio en la mortalidad con TBI pueda deberse a la mejora en el control de la hemorragia por lesiones extracraneales y no a la mejora de la expansión del hematoma intracraneal.
Conclusión del autor: “Los resultados combinados de los dos ECA demostraron una reducción estadísticamente significativa en la progresión de la hemorragia intracraneal con TXA y una mejora no estadísticamente significativa de los resultados clínicos en pacientes de urgencias con TBI. Se requiere más evidencia para respaldar su uso rutinario en pacientes con TBI”.
Punto clínico para recordar: Los resultados de este estudio deben evaluarse cuidadosamente ya que hubo una disminución estadísticamente significativa en la expansión del hematoma intracraneal; esto no condujo a un beneficio de mortalidad estadísticamente significativo ni a una mejora del estado funcional neurológico.
Ácido tranexámico para la hemorragia intracerebral primaria hiperaguda (TICH-2) [4]
Qué hicieron: Este fue un ensayo de fase 3 internacional, aleatorizado, doble ciego, controlado con placebo, de grupos paralelos, de adultos con hemorragia intracraneal por accidente cerebrovascular agudo en 124 hospitales (12 países). Los pacientes fueron aleatorizados de forma 1:1 para recibir 1 g de bolo de TXA intravenoso seguido de una infusión de 1 g de TXA durante 8 horas o un placebo equivalente dentro de las 8 horas posteriores al inicio de los síntomas.
- Intervención: 1 g de TXA en 100 ml de NS infundido durante 10 minutos seguido de otro 1 g en 250 ml de NS infundido durante 8 horas
- Placebo: 100 ml de NS infundidos durante 10 minutos seguidos de otros 250 ml de NS infundidos durante 8 horas
Resultados:
- Primario: estado funcional en el día 90, definido como un cambio ordinal en la escala de Rankin modificada (mRS)
-
Secundario:
- Deterioro neurológico el día 7 o el alta (lo que ocurra primero) evaluado por el NIHSS
- Actividades de la vida diaria según el índice de Barthel
- Costos que incluyen la duración de la estancia hospitalaria.
- Cambio en el volumen del hematoma desde el inicio hasta las 24 horas
- Resultados de seguridad hasta el día 90
- Muerte
- TEV
- Eventos isquémicos (accidente cerebrovascular, AIT, IM, SCA, PAD)
- Convulsiones
Inclusión:
- Adultos con HIC
- Ingresado en un hospital participante dentro de las 8 horas posteriores a la aparición de los síntomas del accidente cerebrovascular (o la última vez que se vio bien)
Exclusión:
- HIC secundaria a anticoagulación, trombólisis, traumatismo o anomalía estructural subyacente conocida
- Contraindicación del TXA
- Dependencia previa al ictus (mRS >4)
- Esperanza de vida <3 meses
- GCS <5
Resultados:
- 2325 pacientes inscritos
- 1161 asignados al azar a TXA
- 1150 recibieron intervención
- 1152 analizados el día 90 Análisis ITT
- 1164 asignados al azar a placebo
- 1157 recibido
- 1155 analizados en el día 90 Análisis ITT
- Tiempo medio desde el inicio del accidente cerebrovascular hasta la aleatorización = 3,6 horas
- Tiempo medio desde la aleatorización hasta el tratamiento = 21 min
- 36 % de los pacientes reclutados en 3 horas
- 1161 asignados al azar a TXA
- Resultado primario: Estado funcional el día 90:
- No hay diferencia entre grupos
- ORa 0,88; IC del 95%: 0,76 – 1,03; p = 0,11
- No hubo diferencias cuando la mRS se dicotomizó en mRS 0-3 frente a 4-6 (aOR 0,82; IC del 95 %: 0,65 – 1,03), p = 0,08).
- Expansión del hematoma el día 2
- TXA: 25%
- Placebo: 29%
- ORa 0,80; IC del 95%: 0,66 – 0,98; p = 0,0300
- Expansión media del volumen del hematoma desde el inicio hasta las 24 horas (ml)
- ATX: 3,72
- Placebo 4,90
- Diferencia de medias ajustada -137 ml; IC del 95%: -2,71 – -0,04; p = 0,0432
- Muerte el día 7
- ATX: 9%
- Placebo 11%
- O 0,73; IC del 95%: 0,53 – 0,99; p = 0,0406
- Muerte por el día 90
- ATX: 22%
- Placebo 21%
- FC 0,92; IC del 95%: 0,77 – 1,10; p = 0,37
- No hubo diferencias en el deterioro neurológico (puntuación NIHSS media en el día 7), resultados funcionales a 90 días, duración de la estancia hospitalaria, disposición al alta, eventos tromboembólicos venosos u oclusiones arteriales.
Fortalezas:
- Hace una pregunta clínicamente importante.
- Ensayo multicéntrico, internacional, aleatorizado, doble ciego, controlado con placebo y de grupos paralelos. Todas las cosas que nos gusta ver en un juicio.
- La asignación del tratamiento se ocultó a los pacientes, a los evaluadores de resultados y a todos los demás trabajadores de la salud involucrados en el ensayo.
- Resultados secundarios y de seguridad preespecificados antes del inicio del ensayo.
- Los grupos estaban equilibrados en las características iniciales.
- Alta adherencia al protocolo del 95% al recibir todo el tratamiento aleatorio.
- Criterios de inclusión amplios que aumentan la generalización en la práctica.
Limitaciones:
- No se recopilaron registros de detección, por lo que no hay datos sobre la elegibilidad.
- Los criterios de inclusión amplios también dieron lugar a una población heterogénea con accidentes cerebrovasculares más graves, mayores volúmenes de hematoma y una mayor proporción de hematomas lobares y hemorragia intraventricular que pueden haber diluido cualquier efecto potencial del tratamiento.
- La mayoría de los pacientes se inscribieron >3 horas después del inicio de la HIC, lo que puede ser otra razón por la que no se observó ningún beneficio con el ATX, ya que estudios previos en trauma han demostrado que se requiere ATX antes de las 3 horas para mejorar la mortalidad.
Discusión:
- Algunas razones principales por las que este ensayo no mostró ningún beneficio:
- Aunque se ha demostrado en la literatura sobre traumatología que ≤3 horas es un período de ventana importante para la eficacia del ATX, este ensayo optó por utilizar 8 horas como ventana de tratamiento para mantener la coherencia con ensayos anteriores de ATX en la HIC traumática. Los ensayos futuros deberían apuntar a una ventana de <3 horas, que es la ventana en la que ocurre la mayor parte del crecimiento del hematoma.
- Los criterios de inclusión amplios son excelentes desde el punto de vista de la generalización, pero en última instancia terminaron siendo una limitación importante en este estudio. Los ensayos futuros deberían considerar la exclusión de pacientes con HIC sin supervivencia o que no se beneficiarán clínicamente de un mayor crecimiento del hematoma.
- Aunque no hubo diferencias en el resultado primario, puede haber alguna señal en todo el ruido. Hubo reducciones en la muerte temprana hacia el día 7 y en la expansión del hematoma, pero ambas deben tomarse como hipótesis generadoras en este momento.
- Nunca he entendido el miedo al tromboembolismo venoso con TXA, ya que es un agente antifibrinolítico, no un agente protrombótico. Este estudio una vez más no muestra ningún aumento en los TEV en el grupo de TXA.
- Un punto importante es que a los pacientes con PAS ≤170 mmHg les fue mejor que a los pacientes con PAS >170 mmHg. La reducción de la presión arterial ha sido la única intervención hasta la fecha para mejorar los resultados funcionales en pacientes con HIC, por lo que el control temprano de la presión arterial es un factor clave para mejorar los resultados de los pacientes.
Conclusión del autor: “El estado funcional 90 días después de la hemorragia intracerebral no difirió significativamente entre los pacientes que recibieron ácido tranexámico y los que recibieron placebo, a pesar de una reducción en las muertes prematuras y los eventos adversos graves. Se necesitan ensayos aleatorios más amplios para confirmar o refutar un efecto del tratamiento clínicamente significativo”.
Punto clínico para recordar: En este ensayo, se administró TXA >3 horas después del inicio del accidente cerebrovascular, los pacientes sufrieron accidentes cerebrovasculares más graves y volúmenes de hematoma más grandes (>60 ml) que en estudios anteriores y, por lo tanto, no sorprende el hecho de que no hubo diferencias en 90 Resultados funcionales al día en pacientes con HIC espontánea que reciben ATX en comparación con placebo.
Conclusión clínica: El ATX no se puede recomendar en este momento en la práctica clínica para la HIC espontánea según los resultados de estos ensayos; sin embargo, algunas hipótesis que generaron resultados incluyeron reducciones en la muerte prematura al día 7 y la expansión del hematoma, y es de esperar que investigaciones futuras intenten responder. estas preguntas.
HPP
Ensayo MUJER [5]
Que hicieron:
- Ensayo aleatorizado, doble ciego y controlado con placebo de mujeres ≥16 años con hemorragia posparto después de un parto vaginal o cesárea en 193 hospitales de 21 países
- Aleatorizado a TXA 1 g IV versus placebo equivalente
- Si el sangrado continuaba después de 30 minutos o se detenía y reiniciaba dentro de las 24 horas, se administraba una segunda dosis de 1 g de TXA o placebo.
Resultados:
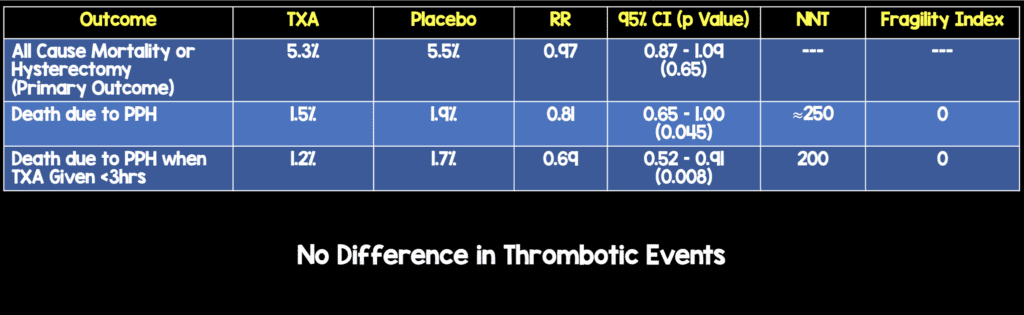
- Primario original: resultado compuesto de mortalidad por todas las causas y/o histerectomía dentro de los 42 días posteriores al parto.
- Resultado primario final: muerte por HPP
Exclusión:
- El médico estaba seguro de que el ATX sería beneficioso o no apropiado
Resultados:
- 20.060 mujeres aleatorizadas
- Grupo TXA: 10.036 incluidos en el análisis
- Brazo de placebo: 9.985 incluidos en el análisis
Fortalezas:
- Ensayo grande, multicéntrico y multinacional
- Participantes, cuidadores y quienes evalúan los resultados cegados a la asignación
- 74% de seguimiento
- Pharma (Pfizer) ayudó a financiar el estudio, pero no participó en el diseño del estudio, la recopilación de datos, el análisis de los datos, la interpretación de los datos ni la redacción del manuscrito final.
Limitaciones:
- Los pacientes se inscribieron en el estudio si los médicos no estaban seguros de si se beneficiarían del TXA. Esto podría subestimar el beneficio del tXA en la HPP.
- El criterio de valoración principal se modificó después del inicio del ensayo.
- El diagnóstico de HPP se realizó clínicamente y no se evaluó la confiabilidad entre evaluadores al tomar esta determinación.
Discusión:
- El criterio de valoración principal se cambió durante el estudio. Los investigadores aprendieron que la decisión de realizar una histerectomía se tomaba con mayor frecuencia en el momento de la aleatorización y, por lo tanto, la intervención no podía afectarla. Sin embargo, el cambio en el criterio de valoración principal se realizó antes de cualquier análisis de datos o desenmascaramiento de datos.
- Al igual que con el estudio CRASH-2, los datos mostraron una asociación consistente entre el retraso en la administración de TXA y ningún beneficio.
Conclusión del autor: “El ácido tranexámico reduce la muerte por hemorragia en mujeres con hemorragia posparto sin efectos adversos. Cuando se utiliza como tratamiento para la hemorragia posparto, el ácido tranexámico debe administrarse lo antes posible después del inicio del sangrado”.
Punto clínico para recordar: El TXA puede o no ser beneficioso para prevenir la muerte por hemorragia en pacientes con HPP sin aumentar el riesgo de TEV. Es difícil sacar conclusiones definitivas de este ensayo ya que el NNT todavía era grande (es decir, ≈250) y el estudio tenía un índice de fragilidad de 0.
Metaanálisis del ensayo CRASH-2 y WOMAN [6]
Que hicieron:
- Este fue un metanálisis de datos a nivel de paciente individual de 2 ensayos aleatorios realizados con más de 1000 pacientes cada uno que evaluó los efectos de los antifibrinolíticos en la hemorragia aguda grave.
Resultados:
- El resultado primario fue la ausencia de muerte por hemorragia y los resultados secundarios de eventos fatales y no fatales por oclusión vascular (IM, accidente cerebrovascular, EP y TVP).
Inclusión:
- Los autores aleatorizaron ensayos controlados con placebo realizados con más de 1.000 pacientes que evaluaron los efectos de los antifibrinolíticos en la hemorragia aguda grave.
Exclusión:
- Se excluyeron los ensayos si eran ensayos en curso sin datos completos o no eran un ensayo aleatorizado controlado con placebo con >1000 pacientes.
Resultados:
- En el análisis se incluyeron 40.138 pacientes de dos ensayos aleatorios de ATX en hemorragia aguda grave (hemorragia traumática y posparto). El ensayo CRASH-2 (Trauma) con 20.127 pacientes y el ensayo WOMAN (hemorragia posparto) con 20.011 pacientes. En total hubo 3.558 muertes en ambos estudios. 1.408 (40%) de las muertes se debieron a hemorragias y 884 de estas muertes (63%) ocurrieron dentro de las 12 horas posteriores al inicio.
- TXA aumentó la supervivencia general durante el sangrado:
- ATX: 96,6%
- Placebo: 96,0%
- TRR: 0,6%
- NNT = 167
- O 1,20; IC del 95%: 1,08 – 1,33; p = 0,001
- Sin aumento de eventos vasculares oclusivos con TXA:
- ATX: 0,2%
- Placebo: 0,3%
- O 0,73; IC del 95%: 0,49 – 1,09
- Efecto del retraso del tratamiento en la supervivencia:
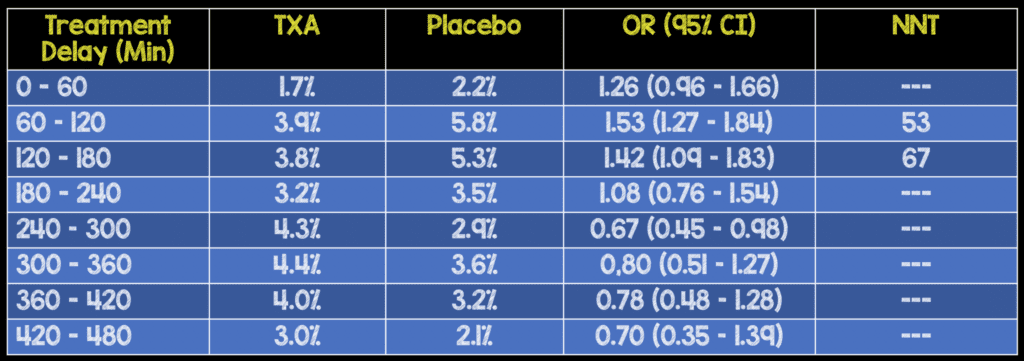
El beneficio de supervivencia se redujo en un 10 % por cada 15 minutos de retraso en el tratamiento hasta las 3 horas, después de lo cual NO hubo BENEFICIO
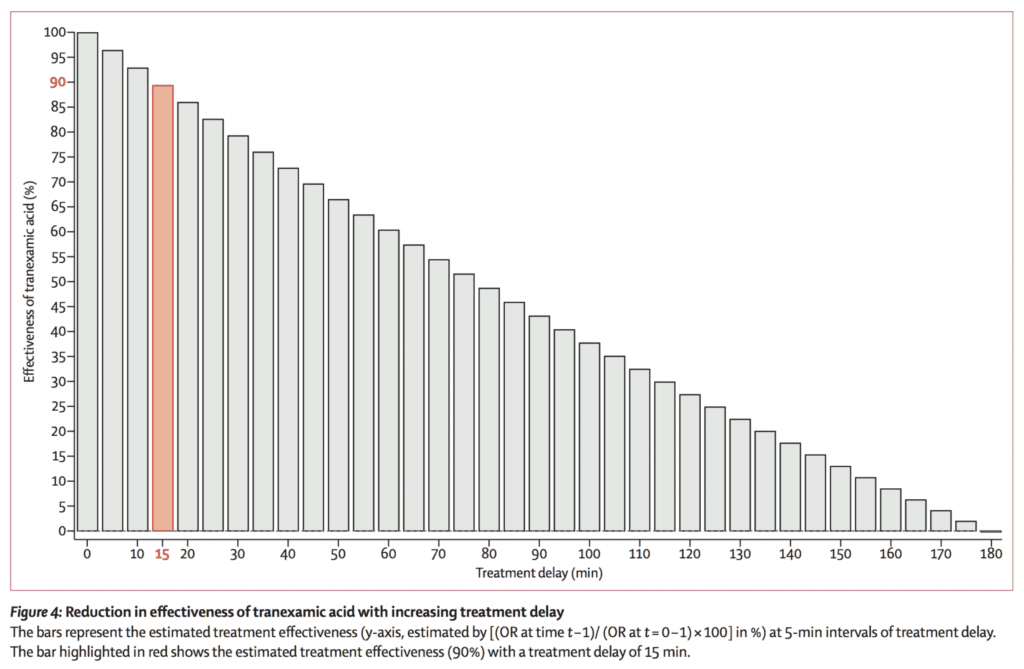
Fortalezas:
- Las mayores fortalezas de este metanálisis fueron la inclusión de ECA de alta calidad controlados con placebo que tuvieron más de 1000 pacientes, lo que ayudó a reducir el sesgo de selección y el resultado primario, que fue la muerte por hemorragia y no la mortalidad por todas las causas, como lo harían los antifibrinolíticos. no afecta otras causas de muerte.
Limitaciones:
- La mayor limitación en ambos ensayos fue que en realidad se desconocía el inicio exacto del sangrado. En CRASH-2 esto puede haber subestimado la efectividad del ATX y en MUJER esto puede haber sobreestimado potencialmente la efectividad del ATX ya que el momento del nacimiento se utilizó como el inicio del sangrado.
Discusión:
- Los autores de este artículo también evaluaron el beneficio relativo del tratamiento observado con intervalos de 60 minutos de retraso del tratamiento desde el momento del inicio del sangrado. No parece haber ningún beneficio adicional cuando se administró TXA en la primera hora, pero también es importante mencionar que una mayor proporción de lesiones penetrantes se observan y tratan en este período de tiempo, y muchas de ellas pueden haber sido lesiones sin supervivencia, por lo que El efecto no parece beneficioso durante esta hora.
Conclusión del autor: “La muerte por hemorragia ocurre poco después del inicio e incluso un breve retraso en el tratamiento reduce el beneficio de la administración de ácido tranexámico. Los pacientes deben ser tratados inmediatamente. Se necesita más investigación para profundizar nuestra comprensión del mecanismo de acción del ácido tranexámico”.
Punto clínico para recordar: en pacientes con sangrado masivo por traumatismo o hemorragia posparto, administrar ATX tan pronto como se sospecha sangrado reduce la mortalidad por sangrado. La mayoría de las muertes, en traumatismos y posparto, por hemorragia, ocurren pocas horas después del inicio del sangrado. El beneficio de mortalidad del TXA parece disminuir con el tiempo y se pierde tres horas después de que comienza la hemorragia importante. En este ensayo, no hubo evidencia de efectos adversos (eventos vasculares oclusivos) asociados con el tratamiento con TXA.
GIBRALTAR
TXA para revisión Cochrane de GIB [7]
Que hicieron:
- Revisión sistemática y metanálisis de ensayos que utilizaron TXA versus ninguna intervención, placebo u otros fármacos antiulcerosos para la gastroenteritis digestiva alta.
Resultados:
- Primario: mortalidad por todas las causas y eventos adversos.
- Secundario: resangrado y cirugía.
Inclusión:
- Ensayos controlados aleatorios, de brazos paralelos, con sospecha de gastroenteritis digestiva alta o verificada endoscópicamente, independientemente de la fuente de hemorragia
Exclusión:
- Enfermedad tromboembólica previa o en curso
- Enfermedad renal crónica
- Pacientes embarazadas
Resultados:
- 8 ECA
- 7 ensayos versus placebo
- 1 ensayo versus ninguna intervención
- 2 ensayos versus fármacos antiulcerosos
- Mortalidad por todas las causas (8 ensayos con 1700 pts):
- ATX: 42/851 (4,9%)
- Placebo: 71/850 (8,4%)
- RR 0,60
- 95% Yo 0,42 – 0,87
- P = 0,007
- Resangrado (7 intentos con 1650 pts):
- ATX: 117/826 (14,2%)
- Placebo: 146/825 (17,7%)
- RR 0,80
- IC 95% 0,64 – 1,00
- P = 0,07
- Ninguna diferencia en los eventos tromboembólicos (solo evaluados en 4 ensayos)
Fortalezas:
- Se contactó a los investigadores del estudio para solicitar los datos faltantes.
- Heterogeneidad clínica y estadística evaluada.
- Se incluyeron pacientes ingresados con sospecha de HD alta confirmada por endoscopia o clínicamente mediante lavado gástrico, hematemesis o melena.
- 7 de 8 ensayos fueron doble ciego con un control de placebo
Limitaciones:
- Muchos pacientes asignados a la aleatorización fueron excluidos posteriormente en algunos estudios (5 de 8 ensayos). Esto dará lugar a un sesgo de desgaste, lo que hará que la calidad general actual de la evidencia sea de moderada a baja.
- Los ensayos incluidos fueron pequeños (es decir, rango: 47 – 204 pacientes), lo que dificulta sacar conclusiones absolutas y, en general, la mediana del número de pacientes por estudio fue de 204 pacientes.
- Sólo tres ensayos incluyeron participantes con hemorragia "grave", lo que puede subestimar el tamaño del efecto total del ATX, ya que cinco estudios se realizaron en pacientes sin hemorragia "grave".
- Un ensayo administró TXA solo por vía intravenosa, tres ensayos administraron TXA VO y los ensayos restantes administraron TXA IV seguido de administración VO
- La dosis diaria total de TXA osciló entre 4 y 8 g y osciló entre 2 y 7 días, lo que no es realista de lo que sucede en un entorno de emergencia aguda.
- Sólo dos ensayos utilizaron el tratamiento endoscópico como tratamiento para la gastroenteritis digestiva alta. En estos ensayos no hubo un beneficio claro sobre el sangrado.
- En varios ensayos, el sangrado por várices fue un criterio de exclusión, lo que dificulta sacar conclusiones sólidas en esta población de pacientes.
Discusión:
- Actualmente, está en marcha el ensayo HALT-IT, que será un ECA de 12.000 pacientes con HD superior que comparará 1 g de TXA IV frente a placebo, seguido de 3 g de TXA infundidos durante 24 horas frente a una infusión de placebo.
- No se pudieron estudiar las necesidades de transfusión porque no se pudieron identificar los datos necesarios
- Una de las razones por las que podemos ver un beneficio en la mortalidad y ningún beneficio en el sangrado es que el ATX solo puede ser beneficioso en pacientes con sangrado "grave" y no en todos los pacientes con gastroenteritis digestiva alta.
Conclusión del autor: "Esta revisión encontró que el ácido tranexámico parece tener un efecto beneficioso sobre la mortalidad, pero una alta tasa de abandonos en algunos ensayos significa que no podemos estar seguros de esto hasta que se publiquen los hallazgos de investigaciones adicionales".
Punto clínico para recordar: Según la mejor evidencia disponible, parece que el ATX en el tracto gastrointestinal superior puede beneficiar la mortalidad en los pacientes más enfermos. (es decir, sangrado masivo, compromiso hemodinámico, pacientes que requieren transfusiones de sangre, etc…). Se necesitan más pruebas de alta calidad para confirmar o refutar estos hallazgos.
Epistaxis
Zahed y otros 2017 [8]
Que hicieron:
- Este estudio fue un ensayo clínico aleatorizado de grupos paralelos realizado en 2 departamentos de emergencia. Un total de 124 pacientes que tomaban fármacos antiplaquetarios (aspirina, clopidogrel o ambos) fueron aleatorizados para recibir ATX tópico (500 mg en 5 ml) o taponamiento nasal anterior.
Resultados:
- El resultado primario de interés fue la proporción de pacientes cuyo sangrado se detuvo a los 10 minutos. Los resultados secundarios fueron la tasa de resangrado a las 24 horas y a la semana, la duración de la estancia en el servicio de urgencias y la satisfacción del paciente.
Inclusión: los pacientes eran elegibles para la inclusión si tenían una hemorragia nasal anterior aguda y tomaban medicamentos antiplaquetarios.
Exclusión: Los pacientes fueron excluidos si la causa de su epistaxis fue traumática, estaban anticoagulados, tenían trastornos hemorrágicos hereditarios, trastornos plaquetarios hereditarios e INR >1,5, shock, un vaso sangrante visible, antecedentes de enfermedad renal y falta de consentimiento.
Resultados: Se evaluó la elegibilidad de un total de 384 pacientes, pero se excluyeron 260 pacientes, dejando solo 124 pacientes disponibles para el análisis. 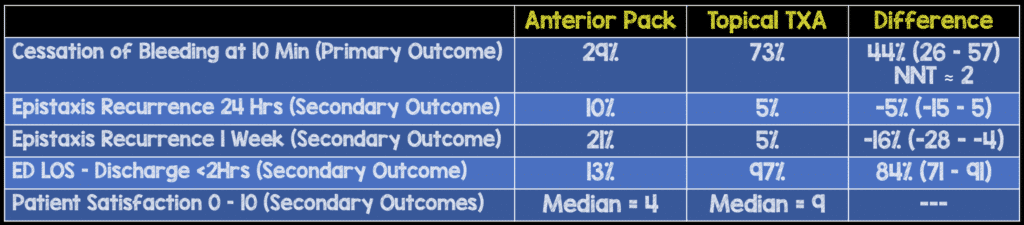
Fortalezas: Los evaluadores de resultados estaban cegados a la asignación del tratamiento.
Limitaciones: Los pacientes con epistaxis posterior no se incluyeron en este ensayo, por lo que no se pueden hacer comentarios sobre el uso de TXA en estos pacientes con base en este estudio.
Discusión: En pacientes con epistaxis anterior, generalmente les pido que se extraigan los coágulos de la nariz, coloquen dos aerosoles de afrin en la fosa nasal afectada, coloquen una compresa empapada en TXA (500 mg en 5 ml) y luego usen una pinza nasal o compresión directa. durante 10 – 15 minutos. Todas estas intervenciones son sencillas y económicas.
Conclusión del autor: "En nuestra población de estudio, el tratamiento de epistaxis con aplicación tópica de TXA dio como resultado un cese del sangrado más rápido, menos resangrado a la semana, una estancia en urgencias más corta y una mayor satisfacción del paciente en comparación con el taponamiento nasal anterior".
Punto clínico para recordar: Según este ensayo, el uso de TXA tópico parece ser superior al taponamiento nasal anterior para el cese del sangrado a los 10 minutos (resultado primario), la duración de la estancia en el servicio de urgencias y la satisfacción del paciente.
Sangrado postamigdalectomía
Metaanálisis 2012 [11]:
Que hicieron:
- Revisión sistemática y metanálisis para evaluar el papel del ATX en la amigdalectomía.
Resultados:
- Pérdida total de sangre (intraoperatoria y posoperatoria)
- Número de pacientes con hemorragia postoperatoria
- Gravedad y duración de la hemorragia.
- Número de pacientes que requieren intervenciones adicionales (ya sean médicas o quirúrgicas)
Inclusión:
- Estudios que utilizan TXA para amigdalectomía durante el período preoperatorio, perioperatorio y posoperatorio
- Diseño de ensayo controlado aleatorio o observacional.
Exclusión:
- Estudios sin grupo control o placebo.
- Pacientes <2 años
- Pacientes con trastornos hemorrágicos.
- Pacientes con adenoamigdalectomía debido a la dificultad para evaluar la pérdida de sangre adicional durante la adenoidectomía específicamente
Resultados:
- 7 estudios con 2.444 pacientes
- 3 ECA
- 4 ensayos de casos y controles
- 2 estudios (180 pacientes) evaluaron el volumen medio de pérdida de sangre
- El ATX disminuyó el volumen medio de pérdida de sangre en 32,72 ml en comparación con el grupo de control.
- IC del 95%: -42,66 a -22,78
- P<0,00001
- 5 estudios (1670 pacientes) evaluaron el número de pacientes con hemorragia postamigdalectomía
- TXA no redujo el riesgo de sangrado post-amigdalectomía
- RR 0,51
- IC del 95%: 0,25 – 1,07
- P = 0,08
- 1 estudio con 40 pacientes evaluó la duración de la hemorragia después de la amigdalectomía
- La duración media del sangrado fue significativamente menor con TXA en comparación con el control a las 3,6 horas.
- 4 estudios informaron efectos adversos y ninguno se encontró en pacientes tratados con TXA
Fortalezas:
- 1ª revisión sistemática y metaanálisis sobre el uso de TXA en pacientes con amigdalectomía
- Estudios incluidos con grupos de estudio y control adecuados.
- Datos extraídos y recopilados por dos revisores independientes para garantizar el acuerdo entre evaluadores en los datos.
- Evaluación de la calidad metodológica completa de todos los ensayos.
Limitaciones:
- La mayoría de los estudios realizados y publicados entre 1970 y 1980
- Estudios incluidos sin falta de cegamiento
- La aplicación de TXA varió en dosis, modo de administración y momento de administración, lo que dificulta identificar una opción de dosificación óptima en pacientes con sangrado postamigdalectomía.
- Ninguno de estos estudios aplicó ATX en el período postoperatorio (todos los estudios investigaron los efectos profilácticos del ATX en pacientes con amigdalectomía, en lugar de los efectos terapéuticos)
- Heterogeneidad significativa de los estudios debido a diferentes criterios de inclusión y exclusión, por lo tanto, diferentes poblaciones de pacientes incluidas en cada ensayo.
Discusión:
- Al evaluar específicamente a los pacientes postoperatorios de amigdalectomía, las vías de administración y las dosis variaron, y solo un estudio evaluó la aplicación tópica (solución tópica de TXA al 4% aplicada durante 4 minutos). En mi práctica estoy nebulizando 500 mg de TXA (basado en datos de hemoptisis)
- Al revisar la literatura, se encontró un único informe de caso pediátrico que extrapolaba el ácido tranexámico nebulizado a partir de estudios de hemorragia alveolar difusa. La dosis es de 250 mg para niños <25 kg, 500 mg para niños >25 kg [12]
Conclusión del autor: "El ATX condujo a una reducción significativa del volumen de pérdida de sangre de la amigdalectomía, pero no tuvo ningún impacto en la tasa de pacientes con hemorragia post-amigdalectomía".
Punto clínico para recordar: en pacientes con sangrado menor post-amigdalectomía, considere usar TXA nebulizado para reducir o detener el sangrado. Los pacientes desangrados no incluidos en estos estudios, aunque son bastante poco comunes, por lo tanto, es difícil sacar conclusiones en esta población de pacientes.
hemoptisis
Informe de caso de ácido tranexámico inhalado 2018 [13]
Que hicieron:
- Este fue el reporte de un caso de un paciente con hemoptisis masiva tratado con ATX nebulizado en el servicio de urgencias. Además, en este artículo se analiza la evidencia del ATX nebulizado en la hemoptisis. Desafortunadamente, por evidencia nos referimos a informes de casos y series de casos. El principal resultado de preocupación es el cese de la hemoptisis. En esta discusión se incluyeron pacientes con hemoptisis masiva (definida como >200 cc durante un período de 24 horas).
Resultados:
- En este artículo se analizan 14 casos individuales de hemoptisis.
- La dosis típica para la hemoptisis oscilaba entre 250 mg y 500 mg de TXA nebulizado, 2 a 4 veces al día, hasta 1000 mg de TXA nebulizado x1.
- El tiempo hasta la resolución de la hemoptisis también osciló entre unos pocos minutos y <72 horas.
- <30min: 7 casos
- 1 – 6hrs: 2 Casos
- 7 – 24hrs: 2 Casos
- 25 – 72hrs: 3 Casos
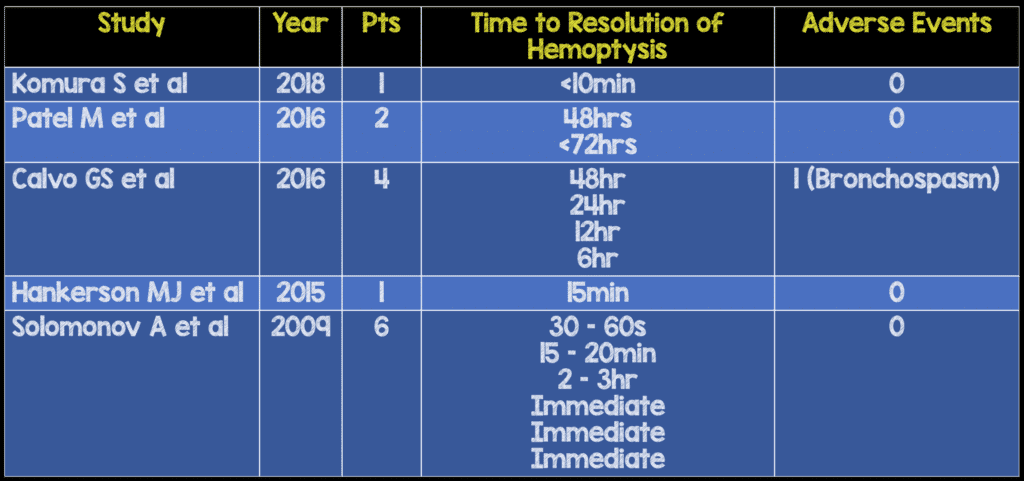
- Resultados adversos: 1 paciente tuvo broncoespasmo, que fue tratado exitosamente con broncodilatadores.
Conclusión del autor: "En la hemoptisis masiva, el ATX nebulizado de rápida disponibilidad puede considerarse una opción terapéutica, ya sea como terapia primaria o como puente hasta que se puedan organizar otras terapias definitivas".
Punto clínico para recordar: El TXA nebulizado en una dosis de 250 mg a 1000 mg, ya sea como medicamento solo o diluido en 20 cc de NS, podría ser un puente para detener o ralentizar la hemoptisis hasta que se pueda llevar a cabo la terapia definitiva. Nuevamente, al igual que con el sangrado postamigdalectomía, los pacientes con compromiso de las vías respiratorias o sangrado masivo no se incluyeron en este análisis. En estos pacientes, la intubación con broncoscopia será la terapia definitiva.
TXA inhalado RCT 2018 [14]:
Que hicieron:
- Ensayo controlado aleatorio prospectivo, doble ciego, controlado con placebo que evalúa la eficacia del TXA nebulizado (500 mg/5 ml tres veces al día) frente a placebo (5 ml de solución salina normal al 0,9%) para el tratamiento de la hemoptisis no masiva
Resultados:
-
Primario:
- Tasa de resolución completa de la hemoptisis durante los primeros 5 días desde el ingreso
- Diferencia en el volumen diario de sangre expectorada.
-
Secundario:
- Tasa de broncoscopia intervencionista
- Tasa de embolización angiográfica
- Tasa de cirugía
- LOS hospitalarios medios
-
Resultado de seguridad:
- Tasa de efectos secundarios
-
Resultados del seguimiento (30 días y 1 año)
- Mortalidad
- Tasa de recurrencia de hemoptisis.
Inclusión:
- Pacientes adultos (≥18 años) ingresados con hemoptisis en las 24 horas previas
Exclusión:
- Hemoptisis masiva (sangre expectorada >200 ml/24 h)
- inestabilidad hemodinámica
- inestabilidad respiratoria
- El embarazo
- Insuficiencia renal (nivel de Cr > 3 mg/dL o necesidad de TRR)
- Insuficiencia hepática (bilirrubina >2 mg/dl o AST > 3 veces el límite superior de lo normal)
- Coagulopatía (INR > 2)
- Hipersensibilidad conocida al TXA
- Tratamiento con TXA previo al cribado
Resultados:
- 47 pacientes aleatorizados
- 25 pacientes recibieron TXA nebulizado
- 22 pacientes recibieron solución salina normal nebulizada
- El 36 % (9 puntos) y el 41 % (9 puntos) tuvieron cáncer de pulmón en el grupo de TXA y en el grupo de placebo, respectivamente.
- >50% de los pacientes fueron tratados con anticoagulantes o antiplaquetarios de forma ambulatoria
- Resolución de la hemoptisis dentro de los 5 días posteriores al ingreso.
- ATX: 96%
- Placebo: 50%
- TAR = 46%
- NNT = 2
- P<0,0005
- La cantidad de sangre expectorada se redujo significativamente el día 2 de ingreso (≈50 cc/24 h frente a 15 cc/24 h)
- Duración media de la estancia hospitalaria
- ATX: 5,7 +/- 2,5 días
- Placebo 7,8 +/- 4,6d
- P = 0,046
- Requerir procedimientos invasivos (es decir, broncoscopia o embolización angiográfica) para controlar el sangrado:
- TXA: 0%
- Placebo 18,2%
- P = 0,041
- No se requirieron procedimientos quirúrgicos en ninguno de los grupos.
- Sin efectos secundarios en ninguno de los grupos, incluido el broncoespasmo.
- Seguimiento a largo plazo:
- Mortalidad a los 30 días:
- TXA: 0%
- Placebo: 10%
- P = 0,21
- Hemoptisis recurrente a los 30d:
- TXA: 8%
- Placebo 27,3%
- P = 0,12
- Mortalidad a los 30 días:
Fortalezas:
- 1er ECA prospectivo para evaluar la eficacia del ácido tranexámico nebulizado en pacientes con hemoptisis
- Tanto el tratamiento como el placebo se prepararon en la farmacia y se suministraron al departamento pulmonar en viales idénticos sin marcar, para permitir el cegamiento del equipo tratante y de los pacientes.
- Los pacientes recogieron sangre expectorada en tazas medidoras diariamente durante el ensayo para medir la cantidad de sangrado, en lugar de cuantificar subjetivamente la cantidad de sangrado.
- Los pacientes estaban equilibrados en cuanto a las características clínicas iniciales y las causas de hemoptisis.
Limitaciones:
- Inestabilidad hemodinámica y respiratoria no claramente definida
- Se excluyeron hemoptisis masiva (>200 cc/h).
- Un pequeño número de pacientes no permite una evaluación específica del ATX nebulizado en diferentes subpoblaciones de hemoptisis (es decir, terapia anticoagulante)
Discusión:
- El estudio requirió que 60 pacientes tuvieran significación estadística y no lo alcanzó con 47 pacientes aleatorizados. Esto se debió a un análisis interno que mostró la superioridad percibida del TXA inhalado frente al placebo después del reclutamiento exitoso de 47 pacientes.
- La principal ventaja del ATX inhalado frente al ATX sistémico en la hemoptisis es un inicio de acción más rápido en el lugar del sangrado.
- También existe una revisión Cochrane de 2016 [15], sin embargo, solo incluyó 2 ECA (uno de 2002 y otro de 1994). El ensayo de 2002 evaluó el ATX oral y el ensayo de 1994 evaluó el ATX intravenoso. Los resultados combinados mostraron una reducción en el tiempo de sangrado en pacientes que recibieron TXA versus placebo, pero con una heterogeneidad significativa.
Conclusión del autor: "Las inhalaciones de TA se pueden utilizar de forma segura y eficaz para controlar la hemorragia en pacientes con hemoptisis no masiva".
Punto clínico para recordar: aunque este fue un estudio pequeño, las ventajas del TXA inhalado frente al placebo en pacientes con hemoptisis no masiva (<200 ml/24 horas) incluyeron una resolución más rápida de la hemoptisis, una estancia hospitalaria más corta, menos procedimientos invasivos y, aunque no estadísticamente, Es significativo, una tendencia hacia una mejora de la mortalidad a los 30 días.
¿Cómo se nebuliza el TXA?

Conclusión clínica del TXA
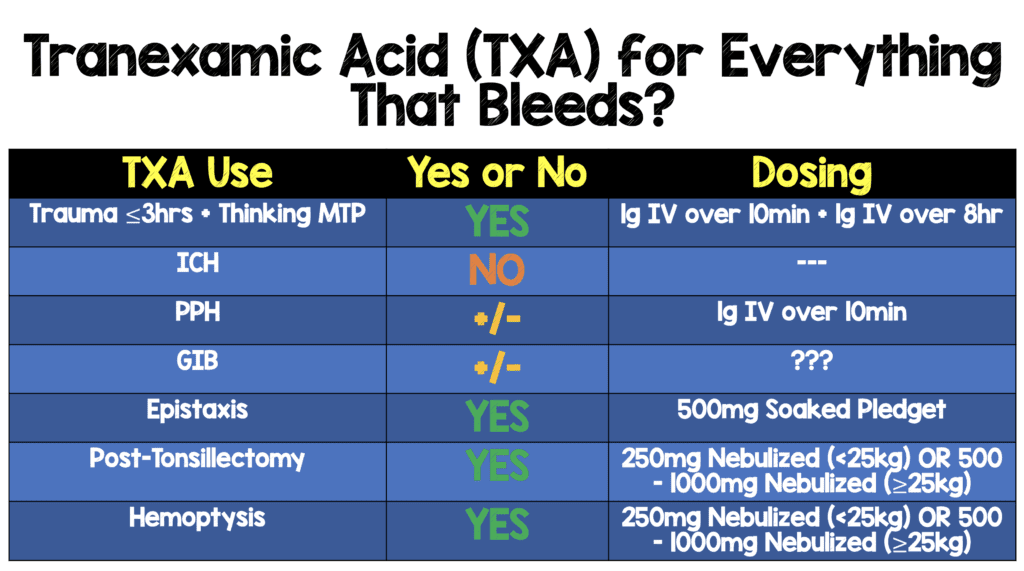
Referencias:
- Morrison J.J. et al. Estudio sobre la aplicación militar del ácido tranexámico en la reanimación de emergencia por traumatismos (MATTERs). Arch Surg 2012. PMID: 22006852
- Shakur H et al. Efectos del ácido tranexámico sobre la muerte, los eventos de oclusión vascular y la transfusión de sangre en pacientes traumatizados con hemorragia significativa. Lanceta 2010. PMID: 20554319
- Zehtabchi S et al. Ácido tranexámico para la lesión cerebral traumática: una revisión sistemática y un metanálisis. Soy J Emerg Med 2014. PMID: 25447601
- Sprigg N y col. Ácido tranexámico para la hemorragia intracerebral primaria hiperaguda (TICH-2): un ensayo internacional de superioridad de fase 3, aleatorizado y controlado con placebo. Lanceta 2018. PMID: 29778325
- MUJER Colaboradoras del Ensayo. Efecto de la administración temprana de ácido tranexámico sobre la mortalidad, la histerectomía y otras morbilidades en mujeres con hemorragia posparto (MUJER): un ensayo internacional, aleatorizado, doble ciego y controlado con placebo. Lanceta 2017. PMID: 28456509
- Gayet-Ageron A et al. Efecto del retraso del tratamiento sobre la eficacia y seguridad de los antifibrinolíticos en la hemorragia aguda grave: un metanálisis de datos individuales a nivel de paciente de 40138 pacientes con hemorragia. Lanceta 2017. PMID: 29126600
- Bennett C y cols. Ácido tranexámico para el sangrado gastrointestinal superior (revisión). Base de datos Cochrane Syst Rev 2014. PMID: 25414987
- Zahed R et al. Ácido tranexámico tópico comparado con taponamiento nasal anterior o tratamiento de la epistaxis en pacientes que toman fármacos antiplaquetarios: ensayo controlado aleatorio. Acad Emerg Med 2017. PMID: 29125679
- José J et al. Ácido tranexámico para pacientes con hemorragia nasal (epistaxis) (revisión). Sistema de base de datos Cochrane Rev 2018. PMID: 30596479
- Chan CC et al. Revisión sistemática y metaanálisis del uso de ácido tranexámico en amigdalectomía. Eur Arch Otorrinolaringol 2013. PMID: 22996082
- Prutsky G et al. Terapia antifibrinolítica para reducir la hemoptisis por cualquier causa (revisión). Sistema de base de datos Cochrane Rev 2012. PMID: 22513965
- Schwarz W et al. Uso de ácido tranexámico nebulizado para la hemorragia secundaria posamigdalectomía en niños. Ann Emerg Med 2019. PMID: 30292524
- Komura S et al. ¿Hemoptisis? Pruebe el ácido tranexámico inhalado. JEM 2018. PMID: 29502864
- Varita O et al. Ácido tranexámico inhalado para el tratamiento de la hemoptisis: un ensayo controlado aleatorio. Cofre 2018. PMID: 30321510
- Prutsky G et al. Terapia antifibrinolítica para reducir la hemoptisis por cualquier causa (revisión). Sistema de base de datos Cochrane Rev 2016. PMID: 22513965
Para obtener más ideas sobre este tema, consulte:
- emDOC: ¡TXA IMPORTA!
- PharmERToxGuy: ácido tranexámico nebulizado (TXA) para el tratamiento agudo de la hemoptisis estable
- REBEL EM: Es hora de utilizar ácido tranexámico (TXA) en hemorragias masivas
Apoye el espectáculo pagando y reclamando 0,75 horas de CME/CEH haciendo clic en el logotipo a continuación
Publicación revisada por pares por: Anand Swaminathan, MD (Twitter: @EMSwami )
El post ¿Ácido tranexámico (TXA) para todo lo que sangra? apareció por primera vez en REBEL EM - Blog de Medicina de Emergencia .

