 El nuevo coronavirus 2019 se informó por primera vez en Wuhan, China, a finales de diciembre de 2019. El brote fue declarado una emergencia de salud pública de importancia internacional en enero de 2020 y el 11 de marzo de 2020, el brote fue declarado pandemia mundial. La propagación de este virus ahora es global y atrae mucha atención de los medios. El virus ha sido denominado SARS-CoV-2 y la enfermedad que causa se conoce como enfermedad por coronavirus 2019 (COVID-19). Este nuevo brote ha estado produciendo mucha histeria y se están difundiendo verdades falsas; sin embargo, los datos sobre la biología, la epidemiología y las características clínicas aumentan diariamente, lo que lo convierte en un objetivo en movimiento. Este post servirá como resumen de una propuesta de estadificación y tratamiento clínico/terapéutico frente al COVID-19.
El nuevo coronavirus 2019 se informó por primera vez en Wuhan, China, a finales de diciembre de 2019. El brote fue declarado una emergencia de salud pública de importancia internacional en enero de 2020 y el 11 de marzo de 2020, el brote fue declarado pandemia mundial. La propagación de este virus ahora es global y atrae mucha atención de los medios. El virus ha sido denominado SARS-CoV-2 y la enfermedad que causa se conoce como enfermedad por coronavirus 2019 (COVID-19). Este nuevo brote ha estado produciendo mucha histeria y se están difundiendo verdades falsas; sin embargo, los datos sobre la biología, la epidemiología y las características clínicas aumentan diariamente, lo que lo convierte en un objetivo en movimiento. Este post servirá como resumen de una propuesta de estadificación y tratamiento clínico/terapéutico frente al COVID-19.
Para volver a la publicación principal, haga clic en la imagen de abajo…
Propuesta de estadificación clínico-terapéutica [8]
La progresión por etapas de la enfermedad COVID-19 puede ayudar en el despliegue y la investigación de la terapia objetivo
- En este editorial los autores proponen un sistema de estadificación clínica para establecer una nomenclatura estandarizada para la evaluación y notificación de enfermedades.
- La farmacoterapia dirigida contra el virus es más prometedora cuando se aplica en las primeras etapas del curso de la enfermedad, pero su utilidad en etapas avanzadas puede ser inútil.
- Es posible que la terapia antiinflamatoria que se aplica demasiado pronto no sea necesaria, ya que la mayoría de las personas solo tendrán una enfermedad leve y se recuperarán sin ninguna dificultad. Esto puede incluso prolongar la replicación viral que se ha descrito con corticosteroides.
- Sistema de estadificación clínica propuesto:
- Etapa I: leve (infección temprana)
- Estadio IIa: moderado (afectación pulmonar sin hipoxia)
- Estadio IIb: moderado (afectación pulmonar con hipoxia)
- Etapa III: grave (hiperinflamación sistémica)
Etapa I leve (infección temprana):
- Esto ocurre en el momento de la inoculación, incubación y establecimiento temprano de la enfermedad.
- Por lo general, se trata de síntomas inespecíficos (es decir, malestar general, tos, fiebre, etc.)
- Dependiendo de dónde trabaje, el diagnóstico se realiza mediante pruebas de RT-PCR respiratoria, pruebas séricas de IgG e IgM del SARS-CoV-2, imágenes de tórax, hemograma completo (es decir, linfopenia, leucopenia, etc.) y LFT.
- El tratamiento debe centrarse en el alivio sintomático.
- Si la terapia antiviral estuviera disponible, este grupo de pacientes podría beneficiarse de reducir la duración de los síntomas, minimizar el contagio y potencialmente la progresión de la enfermedad.
Etapa II: Moderada (afectación pulmonar con y sin hipoxia)
- Esto ocurre con el establecimiento de una enfermedad pulmonar y una inflamación en el pulmón.
- Los pacientes pueden desarrollar neumonía viral, con tos, fiebre y tal vez hipoxia (definida como una PaO2/FiO2 <300 mmHg).
- Las imágenes (CXR y/o TC de tórax) pueden mostrar infiltrados bilaterales u opacidades en vidrio esmerilado.
- El CBC puede tener linfopenia y transaminitis crecientes.
- La procalcitonina suele ser baja o normal en la mayoría de los casos de PNA por COVID-19
- Lo más probable es que estos pacientes necesiten ser hospitalizados para observación y tratamiento.
- El tratamiento volverá a centrarse en medidas sintomáticas.
- En pacientes en estadio IIa (sin hipoxia), se deben evitar los corticosteroides.
- En pacientes en estadio IIb (con hipoxia) y pacientes que requieren ventilación mecánica, la terapia antiinflamatoria podría ser útil, pero se usa con prudencia.
- Algunos lugares pueden tener la posibilidad de utilizar terapia antiviral bajo medidas “compasivas”
Etapa III – Severa (Hiperinflamación sistémica):
- Esta será una minoría de pacientes con COVID-19
- Esto ocurre cuando se produce una hiperinflamación sistémica extrapulmonar (es decir, tormenta de citocinas).
- Se pueden observar elevaciones de IL-2, IL-6, IL-7, factor estimulante de colonias de granulocitos (GCSF), proteína inflamatoria de macrófagos 1-alfa, TNF alfa, PCR, ferritina y dímero D.
- También se pueden ver elevaciones de troponina y BNP.
- En esta etapa, la terapia personalizada dependerá del uso de agentes inmunomoduladores para reducir la inflamación sistémica.
- Los corticosteroides pueden estar justificados junto con inhibidores de citoquinas como tocilizumab (inhibidor de IL-6) o anakinra (antagonista del receptor de IL-1).
- La IVIG también puede desempeñar un papel
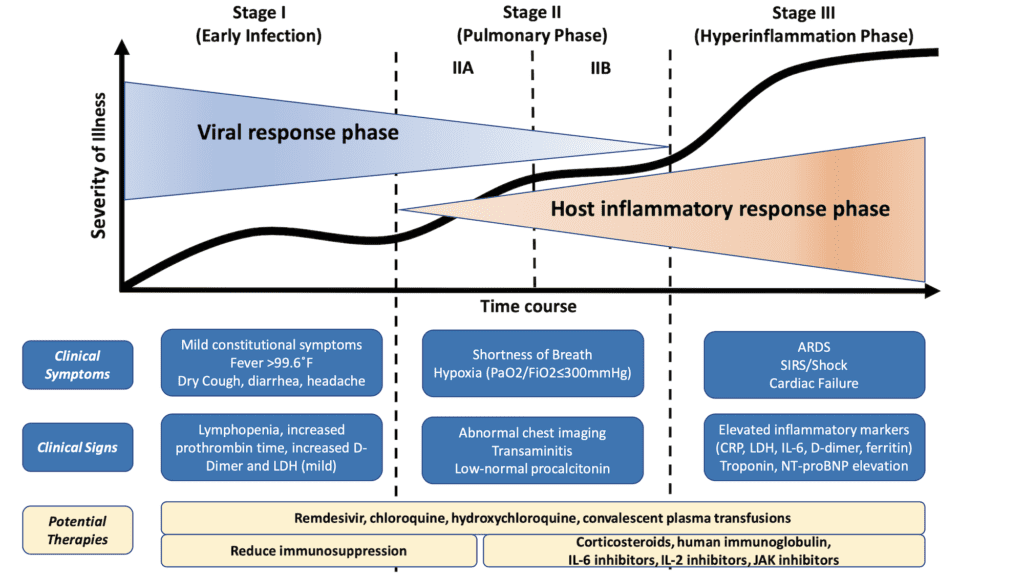
Figura 1: Clasificación de los estados de la enfermedad COVID-19 y posibles objetivos terapéuticos [8][ El enlace está AQUÍ ]
Patogenia hipotética de la COVID-19 [26]
- La inflamación mediada por el sistema inmunológico juega un papel importante en la patogénesis.
- Se ha informado una alta proporción de coagulación aberrante en pacientes graves y críticos con COVID-19, aunque es poco común en otras infecciones por coronavirus, en casos de influenza grave.
- El curso clínico de la infección por SARS-CoV-2 podría dividirse en 3 fases:
- Fase de viremia
- Fase aguda (fase de neumonía)
- Fase grave o de recuperación
- Los pacientes con una función inmune competente y sin factores de riesgo obvios (es decir, edad avanzada, comorbilidades, etc.) pueden generar respuestas inmunes efectivas y adecuadas para suprimir el virus en la primera o segunda fase sin una reacción inmune excesiva.
- Los pacientes con disfunción inmune pueden tener un mayor riesgo de fallar la supresión del virus y, por lo tanto, volverse más graves o críticos con una mayor mortalidad.
- El tratamiento debe centrarse en los factores de riesgo de los pacientes y la ventana de oportunidad puede estar entre la primera y la segunda fase, cuando se afirma deterioro clínico con evidencia de inflamación abrupta y estado de hipercoagulabilidad.
- No existe consenso sobre las mejores opciones de manejo, pero las posibles medidas incluyen:
- Glucocorticoides
- IgIV en dosis altas
- Anticuerpo anti-IL-6R (es decir, tocilizumab, etc.)
- Terapia de plasma convaleciente
- Mensaje para recordar: el momento oportuno es extremadamente importante, independientemente del tratamiento que se pueda utilizar
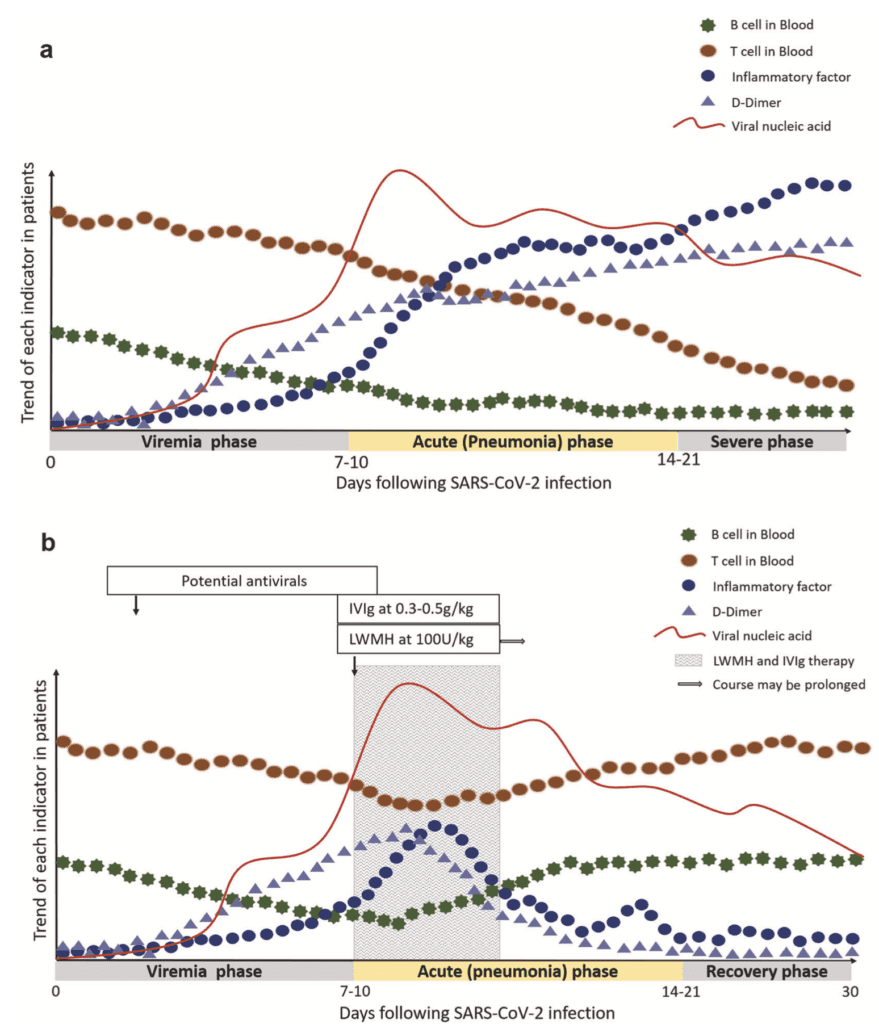
3 fases de la enfermedad (viremia, aguda, grave, recuperación) a lo largo del tiempo frente a la tendencia en las células T/B Factores inflamatorios, dímero D y carga viral en pacientes: A: COVID-19 grave sin tratamiento y B: COVID-19 grave Con tratamiento (HBPM e IGIV)
Tormenta de citoquinas [15][16]
- Se cree que la interleucina-6 (IL-6) es uno de los factores inflamatorios clave en este síndrome.
- La linfohistiocistosis hemofagocítica secundaria (sHLH) es un síndrome hiperinflamatorio caracterizado por hipercitoquinemia fulminante y fatal con insuficiencia multiorgánica.
- Este es un subconjunto de pacientes que tendrán la mayor mortalidad debido a una hiperactividad inmune desregulada.
- Identificar a estos pacientes puede ayudar a predecir qué pacientes se beneficiarían más de la inmunomodulación
Características cardinales:
- Fiebre incesante
- Citopenias
- Hiperferritinemia
- Afectación pulmonar (incluido SDRA)
Detección de hiperinflamación:
- Ferritina elevada (Predictor de mortalidad)
- Plaquetas disminuidas
- VSG elevada
- HScore (la calculadora se puede encontrar AQUÍ )
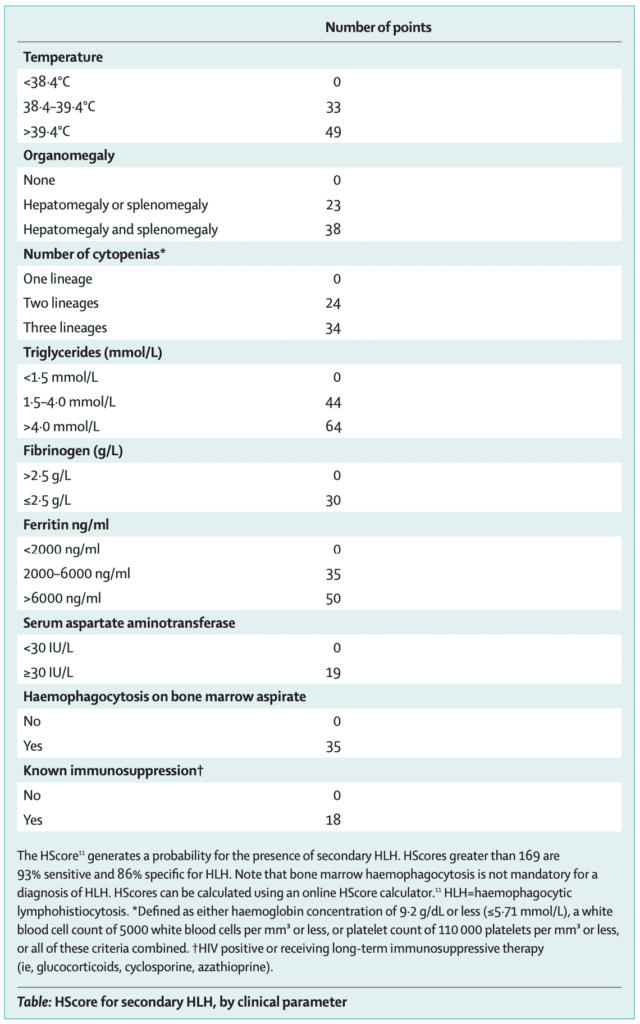
La inmunosupresión en estos pacientes puede beneficiar la mortalidad
- Las opciones incluyen:
- Esteroides (aunque se cree que aumentan la duración de la replicación viral, pueden ser beneficiosos en esta cohorte selecta de pacientes)
- IGIV
- Tocilizumab (inhibidor de IL-6)
Tratamiento/Profilaxis para COVID-19 [1]
[embedyt] https://www.youtube.com/watch?v=EXY76TKNy2Y[/embedyt]
Actualización de COVID-19: marzo de 2020 con el Dr. Anthony Fauci, MD, del 18 de marzo de 2020 (31:39 min)
- Actualmente no existen tratamientos aprobados para ningún coronavirus.
- Actualmente no hay vacuna disponible
- Actualmente no se recomiendan los corticosteroides y actualmente están en estudio ( NCT04273321 )
- Los esteroides pueden prolongar el tiempo de eliminación viral
- Posibles tratamientos que requieren estudio (Basado en estudios en animales, informes de casos/series de pacientes con SARS-CoV y MERS-CoV):
-
Remdesivir:
- Actualmente en estudio ( Clinicaltrials.gov )
- Actividad contra Ébola, MERS y SARS
- Altamente eficaz en un estudio in vitro [3]
- Serie de casos de 61 pacientes con uso compasivo [19]
- Gilead, fabricante de remdesivir, financió y escribió un manuscrito para uso compasivo en COVID-19
- Buscando mejoría clínica (alta hospitalaria viva + disminución de al menos 2 puntos desde el inicio en una escala ordinal modificada)
- Escala ordinal modificada:
- 1 = no hospitalizado
- 2 = hospitalizado
- 3 = hospitalizado, requiriendo oxígeno suplementario
- 4 = hospitalizado, que requiere oxigenoterapia nasal de alto flujo, VNI o ambas
- 5 = hospitalizado, que requiere ventilación mecánica invasiva, ECMO o ambos
- 6 = muerte
- Se inscribieron pacientes con una concentración de O2 ≤94% con aire ambiente O que recibían soporte de O2.
- Ciclo de 10 días de remdesivir (200 mg IV cada día, luego 100 mg una vez al día durante 9 días)
- 61 pacientes recibieron al menos una dosis de remdesivir
- 7 pacientes no tenían datos posteriores al tratamiento
- 1 pt tuvo un error de dosificación
- 53 puntos analizados
- 40 (75%) recibieron el curso completo de 10 días.
- Ventilación Mecánica: 30pts (57%)
- ECMO: 4 puntos (8%)
- Seguimiento medio de 18d
- Soporte de O2 mejorado: 36 puntos (68%)
- Extubados: 17/30 (57%)
- Casa dada de alta: 25/53 puntos (47%)
- Muerte: 7/53 puntos (13%)
- Muerte en pacientes que reciben ventilación mecánica: 6/34 (18%)
- Muerte en pacientes que NO reciben ventilación mecánica: 1/19 (5%)
- Limitaciones:
- Sin cálculo del tamaño de la muestra
- Sin grupo de control
- Más autores que pacientes
- Prueba no ciega
- Selección de puntos poco clara
- Muchos pacientes no están muy enfermos.
- Mejoría clínica observada en 36/53 puntos (68%)
- Dosis sugerida: 200 mg IV x1 día, luego 100 mg IV cada día x9 días [ el enlace está AQUÍ ]
-
Lopinavir/ritonavir:
- Actualmente en estudio ( Clinicaltrials.gov )
- Serie de casos en JAMA (publicada el 3 de marzo de 2020) [2]:
- 5 pacientes que requirieron oxígeno suplementario tratados con lopinavir-ritonavir
- 3 de 5 pacientes mejoraron la fiebre y la necesidad de oxígeno suplementario en 3 días, pero 2 empeoraron con insuficiencia respiratoria progresiva
- 4 de cada 5 pacientes desarrollaron n/v/d
- 3 de cada 5 pacientes desarrollaron LFT anormales
- ECA en NEJM [7]:
- 199 pacientes con infección grave por COVID-19
- No hay diferencias en el tiempo hasta la mejoría clínica (resultado primario)
- Mejora de la mortalidad a los 28 días, estancia en la UCI y porcentaje de pacientes con mejoría clínica a los 14 días (todos los resultados secundarios)
- Se suspendió tempranamente en el 13,8% de los pacientes debido a eventos adversos.
- REBEL EM Deep Dive [ El enlace está AQUÍ ]
- Dosis sugerida: 400-100 mg VO BID x 14 días [ el enlace está AQUÍ ]
-
Cloroquina:
- Medicamentos contra la malaria
- Actualmente en estudio ( Clinicaltrials.gov )
- Altamente eficaz en un estudio in vitro [3]
- Informe inicial: Los resultados de más de 100 pacientes con COVID-19 demostraron que la cloroquina fue superior al tratamiento de control para inhibir la exacerbación de la neumonía, mejorar los hallazgos de las imágenes pulmonares, promover una conversión negativa del virus y acortar el curso de la enfermedad [4]
- ECA preliminar de fase IIb, doble ciego, que analiza diferentes dosis de cloroquina (CQ) para el tratamiento de la neumonía por COVID-19 realizado en Brasil [20]
- Evaluar la seguridad y eficacia de dos dosis diferentes de CQ en pacientes con COVID-19 grave establecido
- Pacientes asignados al azar a 600 mg de CQ dos veces al día x 10 días (dosis total 12 g) frente a CQ 450 mg dos veces al día x 5 días (dosis total 2,7 g)
- Todos los pacientes también recibieron ceftriaxona 1 g dos veces al día durante 7 días, azitromicina 500 mg una vez al día durante 5 días, más oseltamivir 75 mg dos veces al día durante 5 días cuando se sospechaba influenza (89,6% de la población del estudio)
- Tamaño de muestra predefinido de 440 pacientes, 81 pacientes inscritos hasta el momento
- Resultados:
- QTc > 500ms
- CQ de dosis más alta = 25% con tendencia hacia una mayor letalidad 17%
- Debido a una mayor tasa de letalidad, se detuvo prematuramente el reclutamiento de pacientes para este brazo.
- Tasa de mortalidad = 13,5 % (IC del 95 %: 6,9 – 23,0 %) que se superpuso con el IC de datos históricos de pacientes similares que no utilizaron CQ (IC del 95 %: 14,5 – 19,2 %)
- Un ensayo más amplio en curso con un seguimiento de hasta 28 días que busca establecer la letalidad a largo plazo
- Secreción respiratoria negativa para SARS-CoV-2 el día 4 = 1/14pts (7,1%)
- Discusión:
- La CQ se ha asociado con toxicidad retiniana, miopatía y prolongación del intervalo QTc, lo que resulta en arritmias fatales.
- No se pudo utilizar el grupo de placebo; por lo tanto, utilice datos históricos como comparador
- Limitaciones:
- El tamaño limitado de la muestra reclutada hasta el momento no permite mostrar beneficios en cuanto a la eficacia del tratamiento.
- Estudio en un solo centro
- No todos los casos fueron confirmados de COVID-19
- Ausencia de grupo control que utilice placebo.
- Pacientes mayores con CAD asignados aleatoriamente al grupo de dosis alta de CQ
- Conclusión: Los hallazgos preliminares de CloroCovid-19 sugieren que no se deben recomendar dosis más altas de CQ (12 g durante 10 días) en COVID-19
- Dosis sugerida: 500 mg VO BID x10d [ El enlace está AQUÍ ]
-
Tocilizumab:
- Actualmente en estudio ( Clinicaltrials.gov )
- Se une a la IL-6 y bloquea su funcionamiento.
- Potencialmente podría ayudar en pacientes que desarrollan tormenta de citoquinas (implica niveles elevados de IL-6)
- Dosis sugerida: 8 mg/kg en 100 ml de solución NS al 0,9 % IV durante 60 minutos x 1 [ el enlace está AQUÍ ]
-
Hidroxicloroquina:
- Actualmente en estudio ( Clinicaltrials.gov )
- Se descubrió que la hidroxicloroquina es más potente que la cloroquina para inhibir el SARS-CoV-2 in vitro [6]
-
Estudio observacional prospectivo (preimpreso, no revisado por pares) [ El enlace está AQUÍ ]
- 36 pacientes hospitalizados con COVID-19 confirmado
- 26 pacientes recibieron 200 mg de hidroxicloroquina por vía oral tres veces al día x 10 días (6 pacientes también recibieron 500 mg de azitromicina el día 1, 250 mg una vez al día los siguientes 4 días)
- 16 pacientes fueron controles (sin tratamiento). Los pacientes que rechazaron el tratamiento o tenían criterios de exclusión fueron controles
- El día 6 después de la inscripción, el 70% del grupo de tratamiento se curó virológicamente en comparación con el 12,5% en el grupo de control.
- Al comparar la hidroxicloroquina sola con la hidroxicloroquina + azitromicina el día 6 después de la inscripción, el 57,1 % frente al 100 % de los pacientes se curaron virológicamente, respectivamente.
- Sin resultados orientados al paciente (es decir, mortalidad)
- Los resultados son prometedores, pero el tamaño de la muestra es pequeño, el seguimiento de los resultados a largo plazo es limitado y 6 pacientes abandonaron el estudio.
-
Remdesivir:
-
-
- Un estudio piloto realizado en Shanghai [10] aleatorizó a 30 pacientes con COVID-19 a 400 mg de HCQ cada 5 días + tratamiento convencional versus tratamiento convencional solo. No hubo diferencias en su resultado primario de tasa de conversión negativa del ácido nucleico de COVID-19 en un hisopo respiratorio faríngeo 7 días después de la aleatorización. Tampoco hubo diferencias estadísticas en la duración media desde la hospitalización hasta la conversión negativa del ácido nucleico del virus y la progresión radiológica. Hubo un poco más de diarrea y LFT anormales con hidroxicloroquina
-
Pequeño ECA realizado en China (preimpreso, no revisado por pares) [ El enlace está AQUÍ ]
- 62 pts con COVID-19 en China
- Aleatorizado a:
- Adicional 5d HCQ 400mg/d + Tratamiento Estándar
- Tratamiento estándar solo (terapia con O2, agentes antivirales, agentes antibacterianos, IVIG con o sin corticosteroides)
- Tiempo de recuperación clínica a los 6 días
- Tos: 2,0 días frente a 3,1 días
- Recuperación de temperatura: 2,2 días frente a 3,2 días
- PNA mejorada: 80,6% frente a 54,8%
- 2 pacientes con reacciones adversas leves en el grupo HCQ
- Problemas: Pequeños, no cegados, con resultados subjetivos. Los pacientes también recibieron esteroides e IVIG.
-
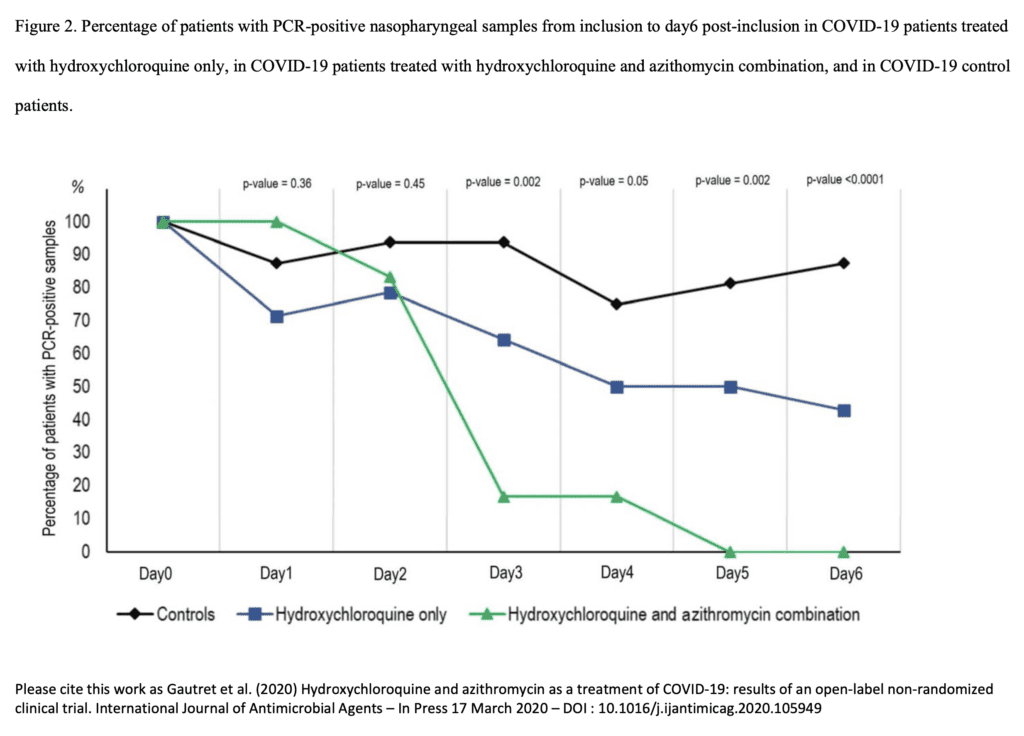
80 pacientes con COVID-19 en Francia (preimpresión, no revisada por pares) [ El enlace está AQUÍ ]
- Recibió una combinación de HCQ 200 mg TID x10d + AZT 500 mg d1 seguido de 250 mg d2 – d4
- Mejoría clínica en 78/80 pts.
- Los cultivos virales fueron negativos en el 97,5% de los pacientes el día 5.
- Problemas: No hay grupo de control
-
1061 pts en Francia con COVID-19 [ El enlace está AQUÍ ]:
- Sólo resumen
- Ensayo observacional de un solo brazo
- Pacientes tratados al menos 3 días con combinación HCQ-AZT + seguimiento al menos 9 días
- Sin toxicidad cardíaca
- Buen “resultado clínico” + Curación virológica = 973 puntos en 10 días (91,7%)
-
Ensayo observacional de 4 hospitales franceses con COVID-19 PNA + que requieren O2 ≥2L/min [22]
- Hidroxicloroquina (HCQ) 600 mg/día en comparación con ninguna HCQ (no aleatorizado)
- Transferencia del criterio de valoración principal compuesto a la UCI dentro de los 7 días posteriores a la inclusión y/o muerte
- 181 puntos
- HCQ dentro de las 48 horas posteriores al ingreso = 84 puntos (17 puntos – 20 % recibieron azitromicina concomitante + 64 – 76 % recibieron amoxicilina/ácido clavulánico concomitantemente)
- Sin HCQ = 97 puntos
- Transferencia a UCI o Muerte dentro de 7 días
- HCQ = 20,2%
- Sin HCQ = 22,1%
- RR 0,91; IC del 95%: 0,47 a 1,80
- Muerte en 7d
- HCQ 2,8%
- Sin HCQ 4,6%
- RR = 0,61; IC del 95%: 0,13 a 2,89
- Desarrollo de SDRA en 7 días.
- HCQ = 27,4%
- Sin HCQ = 24,1%
- RR 1,14; IC del 95%: 0,65 a 2,0
- 8/84 pacientes (9,5%) desarrollaron anomalías en el ECG que requirieron la interrupción de la HCQ
- Discusión:
- En este ensayo, los pacientes no recibieron otros tratamientos antivirales y antiinflamatorios, incluidos esteroides.
- Muchos pacientes tenían PCR > 40 mg/L, lo que puede sugerir que ya había comenzado una tormenta de citocinas (90,5 % en el grupo HCQ y 81,9 % en el grupo sin HCQ)
- Limitaciones:
- No es un ECA, lo que significa que puede haber factores de confusión no medidos
- Número limitado de pacientes con mortalidad.
- La HCQ en diferentes hospitales estaba desequilibrada (algunos centros trataron a todos los pacientes con HCQ, mientras que otros no)
- Conclusión: La HCQ agregada a la atención estándar no se asoció con una reducción de las admisiones a la UCI o la muerte 7 días después del ingreso hospitalario en comparación con la atención estándar sola
-
Ensayo multicéntrico, paralelo, abierto y aleatorizado de 150 pacientes adultos hospitalizados por COVID-19 en China [23]
- HCQ con dosis de carga de 1200 mg una vez al día durante 3 días, seguida de una dosis de mantenimiento de 800 mg durante los días restantes (duración total del tratamiento de 2 a 3 semanas) + atención estándar
- Atención estándar sola
- Criterio de valoración principal = 28 tasa de conversión negativa de SARS-CoV-2
- HCQ: 85,4%
- Sin HCQ: 81,3%
- P = 0,341
- La tasa de conversión negativa en los días 4, 7, 10, 14 o 21 fue similar entre los grupos
- No hay diferencias en la tasa de alivio de los síntomas a los 28 días entre los grupos, pero un alivio más rápido de los síntomas clínicos con HCQ ( segunda semana de enfermedad)
- Los niveles iniciales de PCR y la linfopenia se normalizaron temprano, pero la tasa de mejora general no fue diferente a los 28 días.
- Eventos adversos:
- HCQ: 30%
- Sin HCQ: 8,8%
- Eventos adversos graves: 2 (2,9 %) HCQ frente a 0 (0 %) atención estándar sola
- Evento adverso más común en el grupo HCQ = diarrea (10%)
- Limitaciones:
- Sin resultados orientados al paciente (es decir, mortalidad)
- Estudio no ciego que puede sesgar los resultados subjetivos de los síntomas
- La mayoría de los pacientes con enfermedad leve a moderada (es decir, sólo el 1% con enfermedad grave)
- El juicio terminó antes de tiempo
- Conclusión: HCQ no resultó en una tasa de conversión negativa más alta, pero tuvo un mayor alivio de los síntomas clínicos en comparación con la atención estándar sola
-
Análisis observacional retrospectivo de 368 pacientes evaluados por la Administración de Salud de Veteranos de EE. UU. [25]
- HCQ solo = 97 puntos
- HCQ + AZT = 113 puntos
- Sin HCQ = 158 puntos
- Tasa de muerte:
- HCQ solo = 27,8%
- HCQ + AZT = 22,1%
- Sin HCQ = 11,4%
- Necesidad de ventilación mecánica:
- HCQ solo = 13,3%
- HCQ + AZT = 6,9%
- Sin HCQ = 14,1%
- Conclusión: HCQ con o sin AZT no redujo el riesgo de ventilación mecánica con una asociación de mayor mortalidad general en comparación con ningún HCQ
-
Ensayo observacional de 1376 pacientes [28]
- No se asocia con un riesgo reducido o aumentado de criterio de valoración compuesto de intubación o muerte.
-
Ensayo multicéntrico observacional retrospectivo de 1438 pacientes tratados con HCQ y/o AZT [29]
- No hay diferencias en la mortalidad hospitalaria
-
ECA de 150 pacientes en China [30]
- HCQ + Atención estándar frente a Atención estándar sola
- No hay diferencia en la conversión a RT-PCR negativa del SARS-CoV-2
- Eventos adversos: HCQ 30 % frente a atención estándar sola 9 %
- El evento adverso más común fue la diarrea.
- Dosis sugerida: 400 mg VO BID x1d, luego 200 mg VO BID x4d [ El enlace está AQUÍ ]
-
favipiravir:
- Actualmente en estudio [ Clinicaltrials.gov ]
- Dosis sugerida: 1600 mg VO BID x1d, luego 600 mg VO BID x6d [ El enlace está AQUÍ ]
-
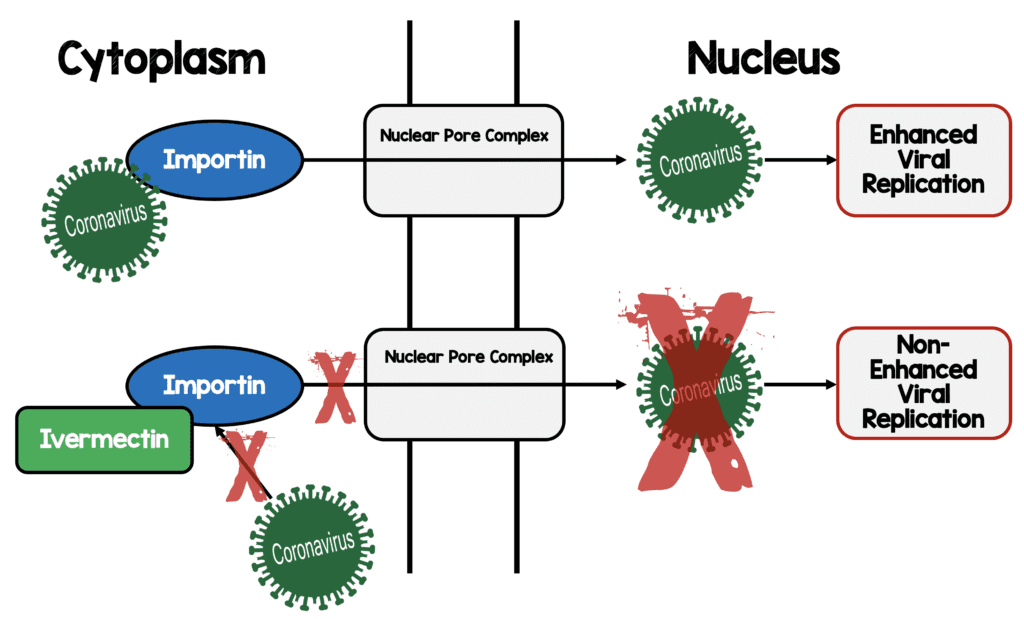
Ivermectina [17]:
- Estudio in vitro de SARS-CoV-2 y dosis única de ivermectina
- 24h = 93% de reducción del ARN viral presente en el sobrenadante
- 24 h = reducción del 99,8 % en el ARN viral asociado a células
- 48 h = reducción de ≈5000 veces del ARN viral en muestras tratadas con ivermectina frente a muestras de control
- No se observó toxicidad en ningún momento.
- Actividad inhibidora del transporte nuclear.
- Estudio in vitro de SARS-CoV-2 y dosis única de ivermectina
-
-
-
Plasma convaleciente [18]:
- 5 pacientes críticos con COVID-19 y SDRA con neumonía grave, carga viral alta, PaO2/FiO2 <300 y ventilación mecánica
- Los pacientes recibieron transfusión de plasma de convaleciente con un anticuerpo específico (IgG) del SARS-CoV-2 los días 10 y 22 después del ingreso.
- La puntuación SOFA disminuyó
- PaO2/FiO2 mejoró en 4/5 pts
- La temperatura corporal disminuyó a lo normal al tercer día
- PCR, Procalcitonina e IL-6 disminuyeron en 4/5 pts
- Los títulos de IgG e IgM aumentaron y permanecieron elevados durante 7 días después de la transfusión.
- 3/5 pts retirados de la ventilación mecánica
- Revisión sistemática de 5 ensayos con 27 pacientes [27]
- 5/5 estudios encontraron reducciones significativas en la carga viral y un aumento de anticuerpos neutralizantes con el tiempo
- Casi todos los pacientes mostraron mejoras en la temperatura corporal, lesiones pulmonares, resolución del SDRA y destete de la ventilación mecánica.
- 5/5 estudios informaron mortalidad cero
- No se produjeron eventos adversos.
- 5 pacientes críticos con COVID-19 y SDRA con neumonía grave, carga viral alta, PaO2/FiO2 <300 y ventilación mecánica
-
Plasma convaleciente [18]:
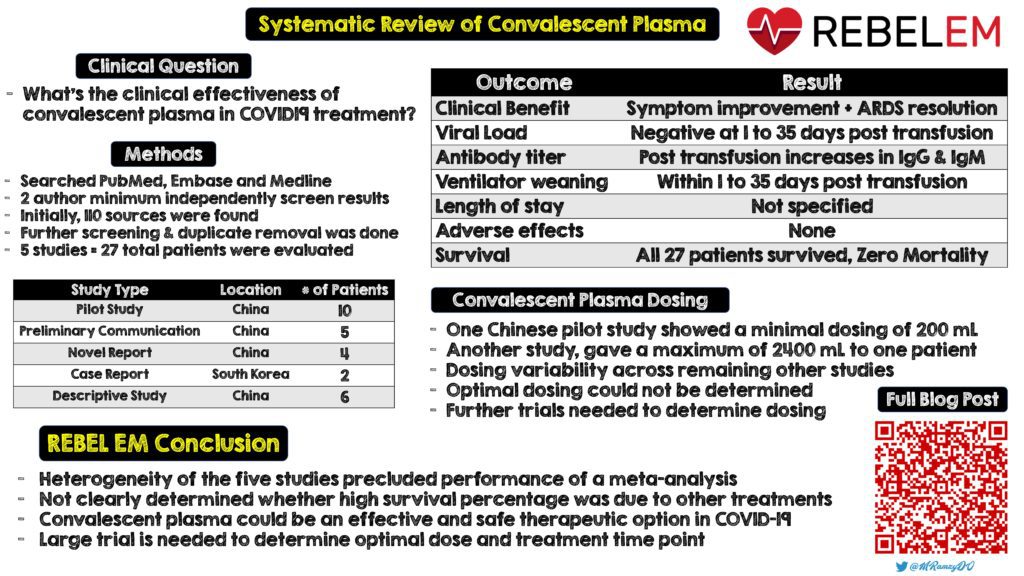
Infografía creada por Mark Ramzy, DO (Twitter: @MRamzyDO )
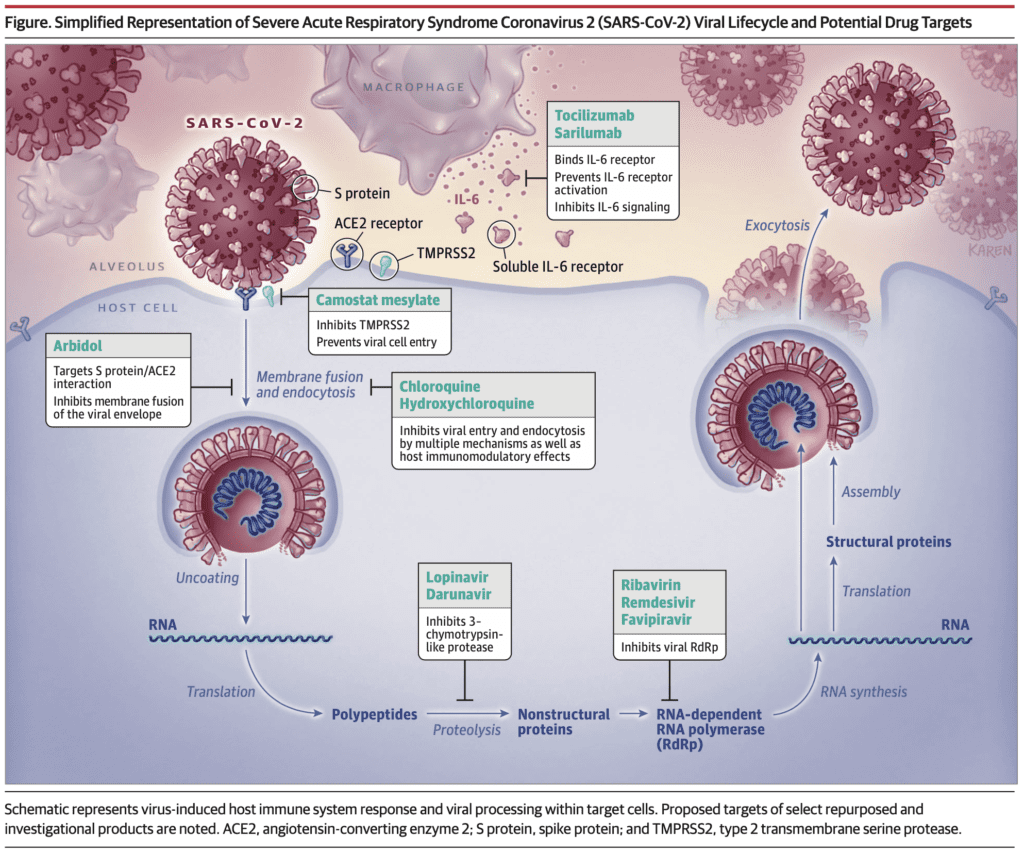
Posibles objetivos farmacológicos de JAMA [21]
IECA/ARAII y COVID19 [5][11][13]:
- El SARS-CoV-2 ingresa a las células pulmonares después de unirse a la membrana ACE2
- ACE1 convierte la angiotensina I en angiotensina II
- ACE2 convierte la angiotensina II en angiotensina
- La angiotensina II es el sustrato conocido de ACE2
- Los niveles plasmáticos de angiotensina II aumentan con la dosificación de BRA
- Los IECA reducen las concentraciones de angiotensina II
- Se ha demostrado un aumento de la expresión de ACE2 con IECA/BRA en los riñones y el corazón, pero no se ha probado en los pulmones.
- El uso de IECA/ARAII podría aumentar la expresión de ACE2 y, por lo tanto, podría aumentar la infectividad del SARS-CoV-2 humano y la gravedad de la enfermedad
- Los datos en humanos son limitados en este momento para respaldar o refutar las preocupaciones sobre los IECA/ARB.
- Estudios poblacionales realizados en China estiman que sólo entre el 30 y el 40% de los pacientes con HTA son tratados con algún tratamiento antihipertensivo y los inhibidores del SRAA se utilizan sólo en el 25 al 30% de estos pacientes tratados [14].
- Existen modelos preclínicos y datos en animales contradictorios sobre los beneficios y daños de los IECA/BRA, pero es posible que estos no se traduzcan en la fisiología humana.
- La recomendación de suspender los BRA no debería ser una práctica común hasta que se confirme esta hipótesis, ya que esto puede provocar una elevación de la PA, lo que podría ocurrir con cambios de tratamiento, y conlleva riesgos que no son hipotéticos.
-
La Sociedad Europea de Cardiología tiene una declaración de posición al respecto del 13/03/2020 [ El enlace está AQUÍ ]:
- La HTA puede estar asociada con un mayor riesgo de mortalidad en pacientes hospitalizados infectados con COVID-19
- Las hipótesis planteadas sugieren un posible efecto adverso de los IECA o los BRA
- La preocupación surge de la observación plausible de que el virus COVID19 se une a ACE2 para infectar células y los niveles de ACE2 aumentan después de IECA/ARB.
- Hay algunos datos en animales que sugieren que estos medicamentos podrían proteger contra complicaciones pulmonares graves en pacientes con infección por COVID19, pero hasta la fecha no hay datos en humanos.
- No existe ninguna base o evidencia científica sólida que respalde esta afirmación.
- "El Consejo sobre Hipertensión recomienda encarecidamente que los médicos y los pacientes continúen el tratamiento con su terapia antihipertensiva habitual porque no hay evidencia clínica o científica que sugiera que el tratamiento con IECA/ARAII deba suspenderse debido a la infección por COVID-19".
-
La Declaración de HFSA/ACC/AHA tiene una declaración de posición al respecto del 17/03/2020 [ el enlace está AQUÍ ]:
- No está claro el papel de ACE2 en el contexto de la infección por COVID-19 en pacientes con enfermedad cardiovascular
- Actualmente no hay datos experimentales o clínicos que demuestren resultados beneficiosos o adversos con el uso de base de IECA, BRA u otros antagonistas del SRAA en COVID-19.
- Recomiendan continuar con los antagonistas del SRAA para aquellos pacientes a los que actualmente se les recetan estos medicamentos y no agregar ni eliminar ningún medicamento relacionado con el SRAA, más allá de las acciones basadas en la práctica clínica estándar.
-
Asociación del uso hospitalario de inhibidores de la enzima convertidora de angiotensina y bloqueadores de los receptores de angiotensina II con la mortalidad entre pacientes con hipertensión hospitalizados con COVID-19 [24]
- Determinar la asociación entre el uso hospitalario de IECA/ARAII y la mortalidad por todas las causas en pacientes con COVID-19 con hipertensión ingresados en 9 hospitales de China
- Estudio retrospectivo, multicéntrico de 1.128 pacientes adultos con HTA diagnosticados de COVID-19:
- Tomando IECA/ARAII: 188
- No tomar IECA/ARB: 940
-
Mortalidad 28d no ajustada:
- Sin IECA/ARAII: 9,8%
- IECA/ARA: 3,7%
- P = 0,01
- uaHR: 0,42; IC del 95%: 0,19 a 0,92; p = 0,03
- FCa: 0,37; IC del 95%: 0,15 a 0,89; p = 0,03
- IECA/BRA también se asoció con una disminución de la mortalidad en comparación con otros fármacos antihipertensivos (aHR 0,30; IC del 95 %: 0,12 a 0,70; p = 0,01
- Conclusión: El uso hospitalario de IECA/ARAII se asoció con un menor riesgo de mortalidad por todas las causas a los 28 días en comparación con los no usuarios de IECA/ARAII. Los resultados fueron emparejados y ajustados para múltiples variables y aún mostraron una asociación con una reducción de la mortalidad por todas las causas en pacientes con HTA.
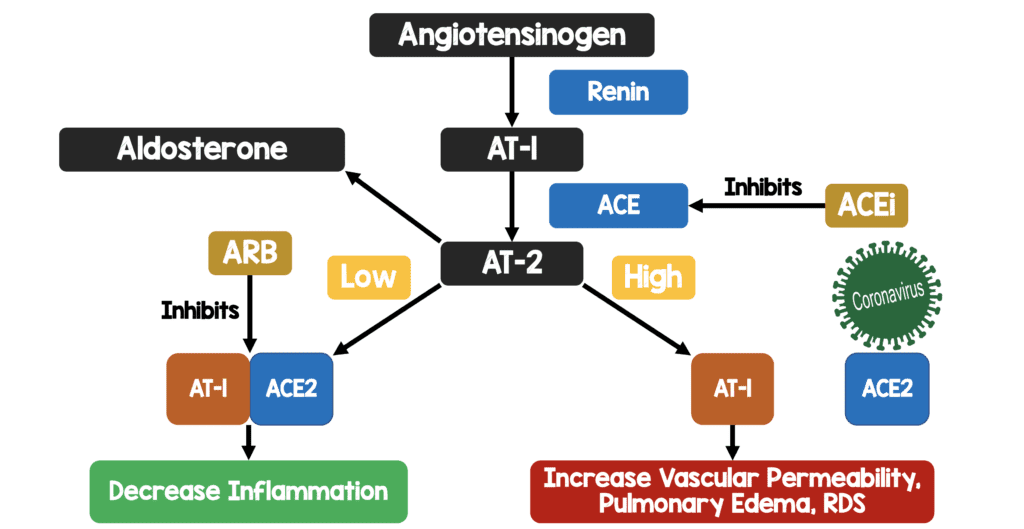
Mi esquema demasiado simplificado de la teoría de la infección ACE2 y COVID19
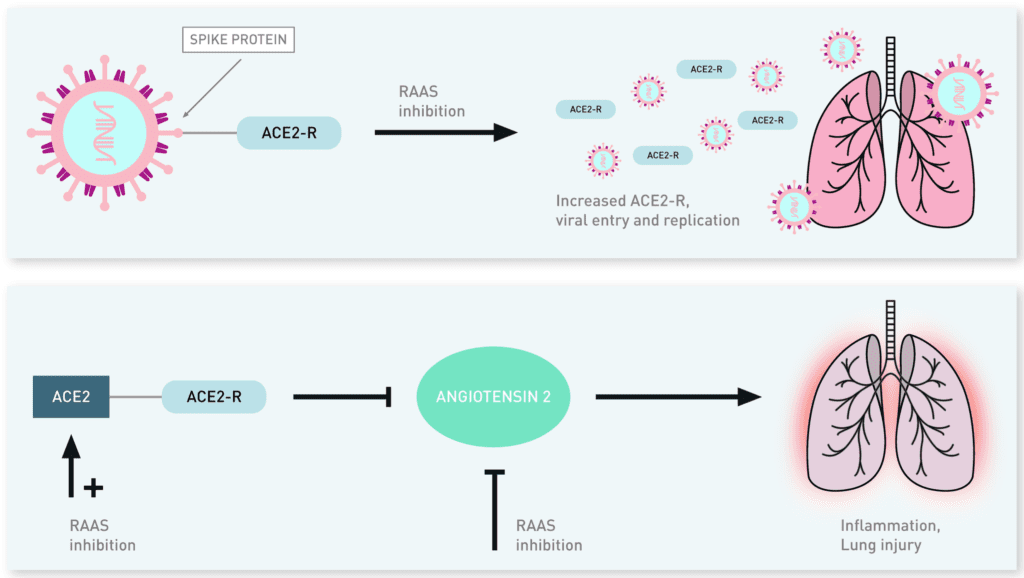
Mecanismos potenciales para ACE2 con respecto a la patogenicidad viral y la protección pulmonar [9]
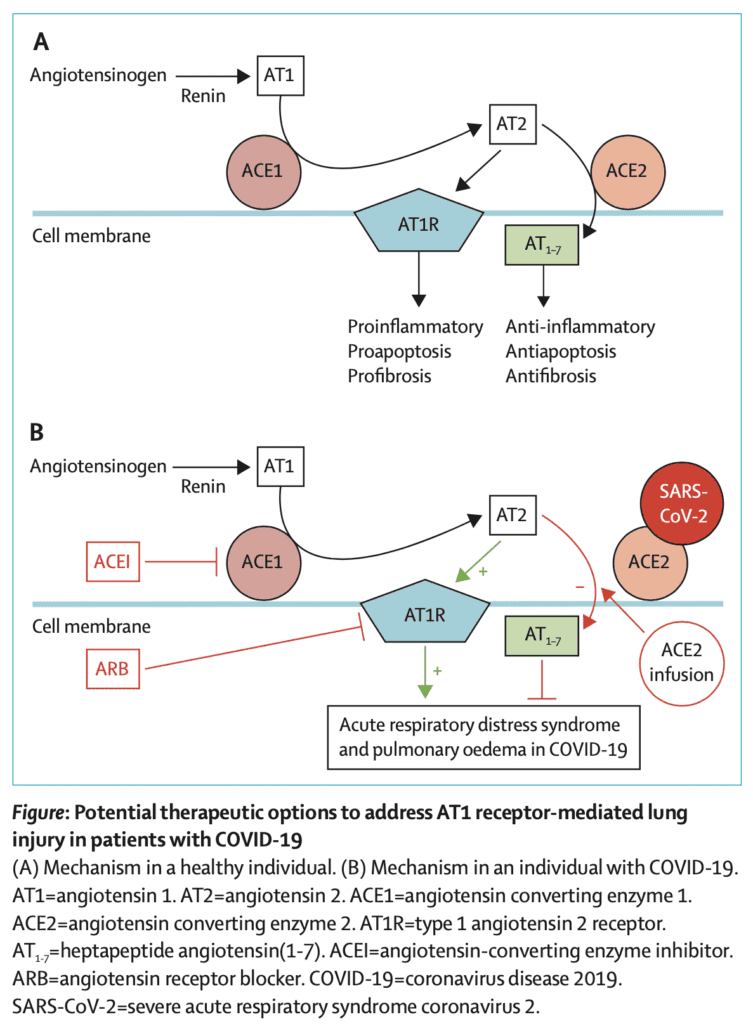
Posibles opciones terapéuticas para abordar la lesión pulmonar mediada por el receptor AT1 en pacientes con COVID-19 (A: mecanismo en pacientes sanos; B: mecanismo en pacientes con COVID-19)[13]
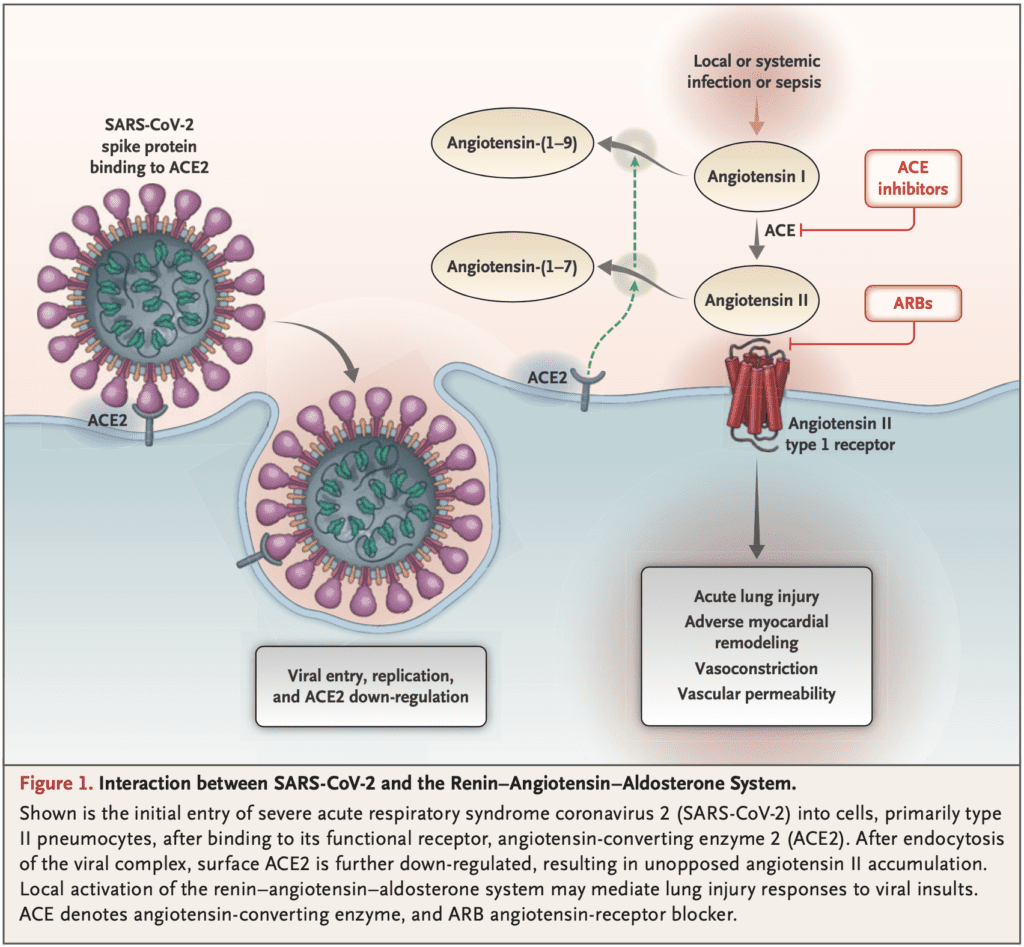
Interacción entre el SARS-CoV-2 y el sistema renina-angiotensina-aldosterona [14]
Ibuprofeno:
- Informes procedentes de Francia indican que el ibuprofeno empeora los efectos del COVID19 (ver tweet a continuación)
- Un informe de The Lancet (el enlace está AQUÍ ) indicó que el ibuprofeno regula positivamente la expresión de ACE2 (el sitio de unión del SARS-CoV-2).
- Aunque existe una explicación biológicamente plausible de que la expresión de ACE2 aumenta con el uso de ibuprofeno, NO hay evidencia sólida en este momento que muestre un empeoramiento de los resultados en la infección por COVID19. Hasta ese momento, se utilizaba paracetamol como antipirético de primera línea en pacientes infectados con COVID19. El ibuprofeno puede empeorar o no los resultados, ya que es una observación que necesitaría un ensayo más amplio para determinar la causalidad. ¿Es posible que estos pacientes estuvieran más enfermos y por eso vemos peores resultados?
#COVIDー19 | El consumo de antiinflamatorios (ibuprofeno, cortisona,…) puede ser un factor de agravamiento de la infección. En caso de incendio, prenez du paracétamol.
Si está usando antiinflamatorios o en caso de duda, consulte con su médico.– Olivier Véran (@olivierveran) 14 de marzo de 2020
P: ¿Podría el #ibuprofeno empeorar la enfermedad de las personas con #COVID19 ?
R: Según la información disponible actualmente, la OMS no desaconseja el uso de ibuprofeno. pic.twitter.com/n39DFt2amF
– Organización Mundial de la Salud (OMS) (@WHO) 18 de marzo de 2020
Por qué el uso de medicamentos no autorizados y el uso compasivo no nos dan respuestas [12]
- Las intervenciones de un solo grupo sin controles concurrentes no conducen a conclusiones definitivas relacionadas con la eficacia o la seguridad.
- La administración de cualquier fármaco no probado como “último recurso” supone erróneamente que será más probable que haya beneficios que daños.
- El uso compasivo de fármacos que no han sido estudiados podría provocar efectos adversos graves
- "La combinación rápida y simultánea de cuidados de apoyo y ECA es la única manera de encontrar tratamientos eficaces y seguros para la COVID-19 y cualquier otro brote futuro"
Referencias:
- Young BE et al. Características epidemiológicas y evolución clínica de los pacientes infectados con SARS-CoV-2 en Singapur. JAMA 2020. [ Publicación electrónica antes de la impresión ]
- Wang M et al. Remdesivir y cloroquina inhiben eficazmente el nuevo coronavirus surgido recientemente (2019-nCoV) in vitro. Resolución celular 2020. PMID: 32020029
- Gao J et al. Avance: el fosfato de cloroquina ha demostrado una eficacia aparente en el tratamiento de la neumonía asociada a la COVID-19 en estudios clínicos. Tendencias Biosci 2020. PMID: 32074550
- Murray E et al. ¿Pueden los fármacos bloqueadores de los receptores de angiotensina ser perjudiciales durante la pandemia de COVID-19? Journal of Hypertension 2020. [ Publicación electrónica antes de imprimir ]
- XY y cols. Actividad antiviral in vitro y proyección del diseño de dosificación optimizado de hidroxicloroquina para el tratamiento del síndrome respiratorio agudo severo por coronavirus 2 (SARS-CoV-2). Clínica Infect Dis 2020. PMID: 32150618
- Cao B et al. Un ensayo de lopinavir-ritonavir en adultos hospitalizados con COVID-19 grave. NEJM 2020. [ Publicación electrónica antes de la impresión ]
- Siddiqi HK et al. Enfermedad COVID-19 en estados nativos e inmunodeprimidos: una propuesta de estadificación clínico-terapéutica. J Trasplante de corazón y pulmón 2020. [ Publicación electrónica antes de la impresión ]
- Driggin E et al. Consideraciones cardiovasculares para pacientes, trabajadores de la salud y sistemas de salud durante la pandemia de la enfermedad del coronavirus 2019 (COVID-19) JACC 2020. [ Publicación electrónica antes de la impresión ]
- Driggin E et al. Consideraciones cardiovasculares para pacientes, trabajadores de la salud y sistemas de salud durante la pandemia de la enfermedad del coronavirus 2019 (COVID-19) JACC 2020. [ Publicación electrónica antes de la impresión ]
- Jun C et al. Un estudio piloto de hidroxicloroquina en el tratamiento de pacientes con la enfermedad común por coronavirus-19 (COVID-19). J Zhejiang Univ (Med Sci) 2020. [ Publicación electrónica antes de la impresión ]
- Patel AB et al. COVID-19 y los inhibidores de la enzima convertidora de angiotensina y el bloqueador de los receptores de angiotensina: ¿cuál es la evidencia? JAMA 2020. [ Publicación electrónica antes de la impresión ]
- Kalil AC. Tratamiento del uso de medicamentos no autorizados, el uso compasivo y los ensayos clínicos aleatorios de COVID-19 durante las pandemias. JAMA 2020. [ Publicación electrónica antes de la impresión ]
- Tignanelli CJ et al. ¿Medicamentos antihipertensivos y riesgo de COVID-19? Lancet Respir Med 2020 [ Publicación electrónica antes de la impresión ]
- Vaduganathan M et al. Inhibidores del sistema renina-angiotensina-aldosterona en pacientes con COVID-19. NEJM 2020. [ Publicación electrónica antes de la impresión ]
- Zhang Chi et al. El síndrome de liberación de citocinas (CRS) del COVID-19 grave y el antagonista del receptor de interleucina-6 (IL-6R) Tocilizumab ser la clave para reducir la mortalidad. Agentes antimicrobianos Int J 2020. PMID: 32234467
- Mehta P et al. COVID-19: Considere los síndromes de tormenta de citocinas y la inmunosupresión. Lanceta 2020. PMID: 32192578
- Caly L et al. El fármaco ivermectina, aprobado por la FDA, inhibe la replicación del SARS-CoV-2 in vitro. Investigación antiviral 2020. [ Publicación electrónica antes de la impresión ]
- Shen C y col. Tratamiento de 5 pacientes críticos con COVID-19 con plasma de convalecientes. JAMA 2020. PMID: 32219428
- Grein J et al. Uso compasivo de Remdesivir para pacientes con COVID-19 grave. NEJM 2020. [ Publicación electrónica antes de la impresión ]
- Silva Borba MG et al. Difosfato de cloroquina en dos dosis diferentes como terapia complementaria de pacientes hospitalizados con síndrome respiratorio severo en el contexto de la infección por coronavirus (SARS-CoV-2): resultados preliminares de seguridad de un ensayo clínico de fase IIb, aleatorizado, doble ciego (estudio CloroCovid-19) ). Preimpresión de MedRxiv [ Publicación electrónica antes de la impresión ]
- Sanders JM et al. Tratamientos farmacológicos para la enfermedad por coronavirus 2019 (COVID-19) Una revisión. JAMA 2020. [ Publicación electrónica antes de la impresión ]
- Mahevas M et al. No hay evidencia de la eficacia clínica de la hidroxicloroquina en pacientes hospitalizados por infección por COVID-19 y que requieren oxígeno: resultados de un estudio que utiliza datos recopilados de forma rutinaria para emular un ensayo objetivo. MedRxiv Preprint 2020 [ Publicación electrónica antes de la impresión ]
- Tang W et al. Hidroxicloroquina en pacientes con COVID-19: un ensayo controlado, aleatorizado y abierto. MedRxiv Preprint 2020. [ Publicación electrónica antes de la impresión ]
- Zhang P et al. Asociación del uso hospitalario de inhibidores de la enzima convertidora de angiotensina y bloqueadores de los receptores de angiotensina II con la mortalidad entre pacientes con hipertensión hospitalizados con COVID-19. Circ Res 2020. PMID: 32302265
- Magagnoli J et al. Resultados del uso de hidroxicloroquina en veteranos estadounidenses hospitalizados con COVID-19. medRxiv 2020 Preimpresión, no revisada por pares [ Publicación electrónica antes de la impresión ]
- Cao W et al. COVID-19: hacia la comprensión de la patogénesis. Investigación celular 2020. [ Publicación electrónica antes de la impresión ]
- Rahendran K et al. Transfusión de plasma de convalecientes para el tratamiento de COVID-19: revisión sistemática. J Med Virol 2020. PMID: 32356910
- Geleris J et al. Estudio observacional de hidroxicloroquina en pacientes hospitalizados con COVID-19. NEJM 2020. [ Publicación electrónica antes de la impresión ]
- Rosenberg ES et al. Asociación del tratamiento con hidroxicloroquina o azitromicina con la mortalidad hospitalaria en pacientes con COVID-19 en el estado de Nueva York. JAMA 2020. PMID: 32392282
- Tang W et al. Hidroxicloroquina en pacientes con enfermedad por coronavirus principalmente leve a moderada 2019: ensayo controlado aleatorio, abierto. BMJ 2020. PMID: 32409561
- Mehra MR et al. Hidroxicloroquina o cloroquina con o sin macrólido para el tratamiento de COVID-19: un análisis de registro multinacional. Lancet 2020. [ Publicación electrónica antes de la impresión ]
Para obtener más ideas sobre este tema, consulte:
- REBEL EM: COVID-19 – El nuevo coronavirus 2019
- FOAMCast: cánula nasal de alto flujo, tormenta de citocinas, transmisión asintomática
- CDC: Información para médicos sobre opciones terapéuticas para pacientes con COVID-19
- DFTB: Inhibidores de COVID y ACE
- First10EM: Cloroquina para COVID: aún no hay buena evidencia
- EM Lit of Note: Actualización sobre hidroxicloroquina y azitromicina
- emDocs: Agentes antivirales: ¿Cuál es su uso en COVID-19?
- First10EM: Antivirales para COVID19: no están listos para uso clínico
- emDocs: Agentes antiinflamatorios y corticosteroides en COVID-19: ¿Cuál es la controversia?
- emDocs: Cloroquina e hidroxicloroquina: ¿tiene valor la COVID-19?
- PulmCrit: 11 razones por las que el artículo del NEJM sobre Remdesivir no revela nada
- PulmCrit: La hidroxicloroquina falla en el primer ECA significativo
- PulmCrit: ¿Uso cronometrado y titulado de esteroides en COVID-19?
- emDocs: La tormenta interior: tormenta de citocinas y COVID-19
- PulmCrit: estudio antes y después de esteroides de corta duración en COVID-19
Publicación revisada por pares por: Anand Swaminathan, MD (Twitter: @EMSwami ) y Mizuho Morrison, DO (Twitter: mizuhomorrison )
The post COVID-19: Propuesta de estadificación clínica/terapéutica y tratamiento apareció por primera vez en REBEL EM - Blog de Medicina de Emergencia .