
 Información previa: La administración de alteplasa (tPA) en el accidente cerebrovascular isquémico agudo (AIS) sigue siendo un tema muy debatido. A medida que los sistemas hospitalarios continúan experimentando cambios importantes para facilitar la administración de este controvertido fármaco, están saliendo más estudios centrados en la neuroimagen y su papel en la ventana temporal del AIS. El ensayo WAKE-UP fue uno de los primeros estudios en identificar patrones de resonancia magnética sugestivos de un accidente cerebrovascular en pacientes cuyo momento de aparición se desconocía. 1,2 Durante los últimos 10 años, otros estudios también han intentado identificar el papel de la neuroimagen avanzada que guía la administración de tPA para mejorar los resultados funcionales. Los autores realizaron un metanálisis para probar la hipótesis de que el tPA mejora los resultados funcionales en comparación con el placebo entre 4,5 y 9 horas después del inicio en pacientes con AIS que recibieron neuroimagen avanzada. Antes de entrar en el estudio, necesitamos comprender mejor la terminología y los diferentes tipos de modalidades de neuroimagen disponibles y cómo desempeñan un papel en los accidentes cerebrovasculares.
Información previa: La administración de alteplasa (tPA) en el accidente cerebrovascular isquémico agudo (AIS) sigue siendo un tema muy debatido. A medida que los sistemas hospitalarios continúan experimentando cambios importantes para facilitar la administración de este controvertido fármaco, están saliendo más estudios centrados en la neuroimagen y su papel en la ventana temporal del AIS. El ensayo WAKE-UP fue uno de los primeros estudios en identificar patrones de resonancia magnética sugestivos de un accidente cerebrovascular en pacientes cuyo momento de aparición se desconocía. 1,2 Durante los últimos 10 años, otros estudios también han intentado identificar el papel de la neuroimagen avanzada que guía la administración de tPA para mejorar los resultados funcionales. Los autores realizaron un metanálisis para probar la hipótesis de que el tPA mejora los resultados funcionales en comparación con el placebo entre 4,5 y 9 horas después del inicio en pacientes con AIS que recibieron neuroimagen avanzada. Antes de entrar en el estudio, necesitamos comprender mejor la terminología y los diferentes tipos de modalidades de neuroimagen disponibles y cómo desempeñan un papel en los accidentes cerebrovasculares.
Terminología:
- Imágenes por tensor de difusión (DTI) = Una herramienta para evaluar órganos cuya estructura es principalmente fibrosa (es decir, el sistema nervioso central y el cerebro).
- Imágenes ponderadas por difusión (DWI) = Combina información funcional con información anatómica obtenida de resonancias magnéticas convencionales para identificar accidentes cerebrovasculares isquémicos. Utiliza DTI para producir detalles significativos de la integridad de la materia blanca
- Imágenes ponderadas por perfusión (PWI) = Cuando se combinan con DWI y angiografía, pueden identificar áreas de isquemia salvables. 3
- Recuperación de inversión atenuada por líquido (FLAIR) = Una secuencia de resonancia magnética avanzada que elimina la señal del LCR y permite la visualización de lesiones cerebrales superficiales. También permite diferenciar entre accidentes cerebrovasculares isquémicos e infartados. 4
- Desajuste de perfusión-difusión: una anomalía del volumen extremadamente dependiente del tiempo entre DWI y PWI que proporciona una medida práctica y aproximada del tejido en riesgo en el accidente cerebrovascular isquémico. 5
Pregunta clínica:
- ¿La alteplasa intravenosa mejora los resultados funcionales en comparación con el placebo en pacientes con accidente cerebrovascular isquémico entre 4,5 y 9 horas después del inicio o del accidente cerebrovascular al despertar a quienes se les tomaron imágenes con TC de perfusión o resonancia magnética de perfusión-difusión?
Que hicieron:
- Revisión sistemática y metanálisis de datos de pacientes individualizados para ensayos que utilizaron Alteplase con placebo (0,9 mg/kg, máximo de 90 mg administrados en forma de bolo al 10 % y infusión del 90 % durante 1 hora) publicados en inglés entre el 1 de enero de 2006 y el 1 de marzo. 2019 utilizando los siguientes términos de búsqueda:
-
- "Ataque"
- “Aleatorizado” o “Aleatorizado”
- “Trombólisis”
- “Alteplasa” o “tPA”
- Los autores también revisaron la lista de referencias de revisiones sistemáticas anteriores sobre trombólisis.
- También se realizaron búsquedas en ClinicalTrial.gov para estudios intervencionistas sobre accidente cerebrovascular isquémico.
- Los autores identificaron los siguientes tres estudios que cumplieron con los criterios de inclusión: EXTEND, ECASS-4:EXTEND y EPITHET (ver Tabla 1).

- Los investigadores de los tres estudios acordaron agrupar los datos clínicos y de imágenes de cada paciente para utilizarlos en este metanálisis.
- Los autores utilizaron la puntuación de Rankin modificada (mRS) para evaluar la mejora funcional, la independencia y los resultados (ver Tabla 2).

Criterios de inclusión:
- Aleatorizado
- Multicéntrico
- doble ciego
- Edad ≥ 18 años
- Ensayos de 2 brazos con aleatorización 1:1 de alteplasa intravenosa frente a placebo
- Pacientes con >4,5 horas desde el inicio o después del último episodio conocido
- Imágenes adquiridas antes del tratamiento con resonancia magnética de perfusión-difusión o perfusión por TC
- Pacientes con datos disponibles sobre lo siguiente:
- Edad
- Escala de accidentes cerebrovasculares de los Institutos Nacionales de Salud previo al tratamiento (NIHSS)
- mRS a los 3 meses
Criterio de exclusión:
- Cualquier estudio en el que los pacientes no recibieron perfusión por TC ni imágenes por resonancia magnética de perfusión-difusión.
Resultados:
Primario:
- Resultado funcional determinado por una puntuación mRS 0 – 1 a los 3 meses
- Ajustado según la gravedad clínica previa al tratamiento mediante NIHSS y edad
Secundario:
- Mejora funcional, determinada por una reducción de ≥1 punto en la puntuación mRS con las categorías 5 y 6 fusionadas a los 3 meses (análisis de turnos ordinales)
- Independencia funcional, determinada por una puntuación mRS de 0 – 2 a los 3 meses
- Mejoría neurológica temprana determinada por una reducción de ≥ 8 puntos en la NIHSS o alcanzar una puntuación NIHSS de 0 a 1 a las 72 horas
- Todos los resultados secundarios enumerados anteriormente se ajustaron según la gravedad clínica previa al tratamiento mediante NIHSS y la edad.
Seguridad:
- Hemorragia intracerebral sintomática definida como un coágulo de sangre que ocupa >30% del territorio infartado con un efecto de masa sustancial dentro de las 36 horas posteriores al tratamiento.
- Deterioro neurológico de ≥4 puntos NIHSS o muerte
Resultados:
- Tres ensayos cumplieron los criterios de elegibilidad: EXTEND, ECASS4-EXTEND y EPITHET
- Hubo un total de 414 pacientes en los tres ensayos.
- 213 (51%) fueron asignados para recibir alteplasa
- 201 (49%) recibieron el placebo
- La mediana del tiempo desde el último pozo conocido hasta el tiempo de tratamiento en pacientes con accidente cerebrovascular al despertar fue de 10 horas y 42 minutos (RIC 8 horas 40 minutos – 12 horas y 20 minutos)
- La mediana del desajuste de perfusión fue de 47 ml (RIC 17 – 85) con un volumen mediano de hipoperfusión crítica de 64 ml (30 – 109) y un núcleo relativamente pequeño con un volumen mediano de 8 ml (0 – 22) (es decir, infarto de núcleo pequeño con núcleo grande penumbra isquémica ).
- 211 pacientes del grupo de alteplasa y 199 pacientes del grupo de placebo tenían datos de mRS disponibles a los tres meses y se incluyeron en los resultados de resultados primarios.
- El estado de desajuste de perfusión utilizando un software automatizado fue posible en 405 pacientes y 304 pacientes tuvieron un desajuste de perfusión.
- 152 (73%) de 207 en el grupo de alteplasa
- 152 (77%) de 198 en el grupo de placebo
- En total, de los 403 pacientes con imágenes angiográficas evaluables, 246 (61%) tenían oclusión de grandes vasos que potencialmente sería susceptible de trombectomía endovascular.
- 76 (36%) de los 211 en el grupo de alteplasa lograron el resultado primario en comparación con 58 (29%) de los 199 en el grupo de placebo.
Resultados críticos:

- Diez (5%) de los 213 pacientes que recibieron alteplasa tuvieron hemorragia intracerebral sintomática en comparación con un paciente de 201 en el grupo de placebo.
- No se identificaron diferencias significativas en la mortalidad entre los 29/213 (14%) pacientes que recibieron alteplasa y los 18/201 (9%) pacientes en el grupo de placebo (OR 1,55, IC 95% 0,81-2,96, p = 0,19).
- No se identificaron diferencias significativas en la proporción de pacientes con puntuaciones mRS combinadas de 5 o 6. 48 (23%) de 211 en el grupo de alteplasa frente a 41 (21%) de los 199 pacientes en el grupo de placebo (OR ajustado 1,03, 95 % IC 0,62-1,74, p = 0,897)
- Se produjo hemorragia intracerebral fatal en el 2,3% de los pacientes en este análisis.
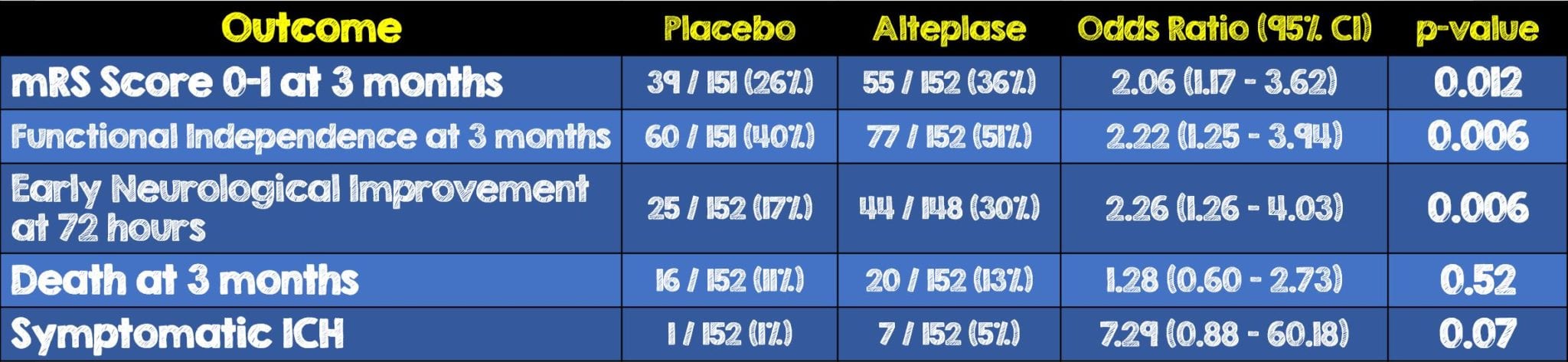
- Entre una subcohorte de la población de pacientes más grande, 303 pacientes con desajuste de perfusión automatizada que tenían puntuaciones mRS disponibles a los 3 meses, 55 (36%) de los 152 pacientes en el grupo de alteplasa lograron un resultado funcional excelente en comparación con los 39 (26%) de los 151 en el grupo placebo (OR 2,06, IC 95% 1,17-3,62, p = 0,012)
- Entre los pacientes con desajuste de perfusión automatizada, se observaron mejoras significativas en todos los resultados secundarios en el grupo de alteplasa en comparación con el grupo de placebo.
- En los pacientes sin discrepancia, no hubo diferencias significativas entre los dos grupos.
- La selección automatizada de desajustes de perfusión no pareció alterar el riesgo de hemorragia intracerebral sintomática en el grupo de alteplasa en comparación con todos los pacientes.
Fortalezas:
- Los investigadores y los comités de gestión de los tres estudios contaron con un estadístico que reunió todos sus datos para los fines de este metanálisis (los comités de gestión de todos los ensayos incluidos acordaron compartir datos a nivel de paciente individual para los fines de este metanálisis)
- Los autores del estudio utilizaron un amplio rango de fechas, muchos términos de búsqueda e incluso buscaron en ensayos clínicos actuales estudios de intervención sobre accidente cerebrovascular isquémico para que este metanálisis fuera lo más completo posible.
- La adjudicación central del estado de desajuste de perfusión utilizando el software RAPID automatizado fue posible en 405 pacientes (los datos de imágenes sin procesar no estaban disponibles para seis pacientes en el grupo de alteplasa y tres pacientes en el grupo de placebo)
- Dos revisores evaluaron de forma independiente los artículos para su inclusión.
- Se intentó subdividir la escala de Rankin modificada en definiciones de resultados prácticos relacionados con la función y la independencia de un paciente.
- Se tuvo en cuenta la varianza entre los ensayos mediante el uso de un modelo de regresión logística de efectos mixtos que se incorporaron como efectos aleatorios en todos los modelos.
- Se utilizó un neurólogo en accidentes cerebrovasculares con amplia experiencia en análisis de neuroimágenes que no conocía la asignación del tratamiento ni toda la demás información clínica para verificar visualmente y eliminar los artefactos de las imágenes.
- Boehringer Ingelheim proporcionó los productos del estudio de investigación de forma gratuita, sin embargo, no participó en el diseño del estudio, la redacción del protocolo, la recopilación, el análisis o la interpretación de los datos.
Limitaciones:
- Dos de los tres estudios (EXTEND y ECASS4-EXTEND) finalizaron prematuramente debido a factores externos. Esto limita el tamaño general de la muestra.
- Todos los pacientes fueron reclutados en Australia, Nueva Zelanda, Europa y Asia, que tienen sistemas de atención médica diferentes en comparación con los Estados Unidos. Esto puede limitar los resultados de este estudio a un sistema de salud de los Estados Unidos.
- Las imágenes de perfusión no están disponibles en muchas regiones y hospitales en general, lo que limita la validez externa y la reproducibilidad de este estudio.
- Estudio dirigido a un subconjunto muy reducido de instituciones que no cuentan con trombectomía endovascular, pueden administrar trombólisis y cuentan con neuroimagen avanzada ponderada por difusión y perfusión.
- Los autores informan que el software automatizado disponible comercialmente que utilizaron es costoso y aún requiere supervisión médica. Esto restringe la generalización del estudio a instituciones más ricas en recursos.
- Este metanálisis se realizó antes de que se publicara la evidencia que respaldaba la trombectomía endovascular. El 97 % de los pacientes (403 de 414) fueron reclutados antes de que se realizara este cambio en las directrices en febrero de 2018, recomendando la trombectomía en el período de 6 a 24 horas. Como resultado, la consideración de la trombectomía fue un criterio de exclusión en los tres ensayos incluidos.
- La puntuación inicial del NIHSS no es igual en ambos grupos: mediana de la puntuación del NIHSS 12 [RIC 7-17] frente a 10 [6-16], pero no es estadísticamente significativa
- El análisis no tuvo suficiente poder para detectar una interacción estadística entre el estado de discrepancia y el efecto del tratamiento. La magnitud de la diferencia en las estimaciones puntuales sugiere que el efecto se debe a que los pacientes cumplen con los criterios de desajuste de perfusión.
Discusión:
- Esta es la primera revisión de metanálisis que combina varios estudios que utilizaron neuroimagen avanzada para determinar el beneficio de la administración de tPA en un período de tiempo de accidente cerebrovascular de 4,5 a 9 horas y despertar accidentes cerebrovasculares.
- Los autores informan que su revisión de la literatura comenzó en el año 2006 porque fue el año en que se describió la trombólisis en pacientes con desajuste en la perfusión-difusión en el estudio no aleatorizado DEFUSE.
- Si bien la escala de Rankin modificada es un sistema de puntuación ampliamente aceptado que se utiliza para categorizar varios niveles de discapacidad, todavía existe una zona gris importante en su aplicación general a todos los pacientes. “Alguna ayuda” o “asistencia” varía en su significado y aplicación práctica para los pacientes y sus actividades diarias.
- El concepto de falta de coincidencia no puede subestimarse aquí: si el núcleo del infarto de un paciente es grande y la porción isquémica es pequeña, entonces probablemente tendrá una pequeña posibilidad de beneficiarse. Lo contrario es cierto, si el núcleo del infarto es pequeño y su porción isquémica es grande, hay más posibilidades de beneficio. La tasa de hemorragia intracerebral sintomática sigue siendo la misma independientemente de si no coinciden o no.
- Los pacientes que cumplieron con los criterios automatizados de discrepancia tuvieron un beneficio significativo de la alteplasa en términos de resultado funcional e independencia y mejoría neurológica. Este beneficio no alcanzó significación estadística en pacientes sin desajuste de perfusión. Además, no se identificó ninguna interacción estadísticamente significativa entre el estado de discrepancia y el efecto del tratamiento.
- Los intervalos de confianza en este análisis fueron muy amplios y cercanos a cero. No está claro si los resultados seguirían siendo estadísticamente significativos si tuviera una población de pacientes más grande.
- En comparación con estudios anteriores en los que se administró alteplasa dentro de la ventana de inicio del accidente cerebrovascular de 0 a 3 horas, el OR ajustado para lograr una puntuación mRS de 0 a 1 entre todos los pacientes fue de 1,75 (IC del 95 %, 1,35 a 2,27), para la alteplasa administrada en la ventana de inicio del accidente cerebrovascular de 3 a 4,5 horas 1,26 (IC del 95 %, 1,05 a 1,51). 6 En este análisis, el OR ajustado fue de 1,86 (IC del 95 %: 1,15 – 2,99) entre todos los pacientes y de 2,06 (IC del 95 %: 1,17 – 3,62) para los pacientes con desajuste de perfusión automatizada.
- El efecto del tratamiento con alteplasa fue numéricamente menor que el observado con la trombectomía endovascular (18% de diferencia en la puntuación mRS 0 – 1). 7,8
- Más de la mitad de los pacientes tenían oclusión de grandes vasos que habría sido susceptible de tratamiento con alteplasa sistémica. Como se mencionó anteriormente, el 97 % de los pacientes fueron reclutados antes de que se realizaran los cambios en las pautas de trombectomía de febrero de 2018 y, por lo tanto, la consideración de la trombectomía fue un criterio de exclusión en los tres estudios. En la práctica actual, el 61% de los pacientes en este análisis serían elegibles para trombectomía debido a la presencia de una oclusión proximal de un gran vaso. El uso combinado de trombólisis y trombectomía endovascular en un período de tiempo prolongado se está investigando actualmente en un ensayo activo y en curso (NCT03785678 ).
Conclusiones del autor:
- Los pacientes con accidente cerebrovascular isquémico entre 4,5 y 9 h desde el inicio del accidente cerebrovascular o accidente cerebrovascular al despertar con tejido cerebral recuperable que fueron tratados con alteplasa lograron mejores resultados funcionales que los pacientes que recibieron placebo. La tasa de hemorragia intracerebral sintomática fue mayor con alteplasa, pero este aumento no anuló el beneficio neto general de la trombólisis.
Nuestra conclusión:
- Para los pacientes sin oclusión de grandes vasos, estos datos impulsan a ampliar el número de pacientes con AIS que pueden beneficiarse de la alteplasa sistémica. (es decir, ventana de 4,5 a 9 horas + pulsaciones para despertar). La independencia funcional es un resultado subjetivo que varía de un paciente a otro y es difícil de categorizar con un único sistema de puntuación. Además, no todas las instituciones tienen acceso a las modalidades avanzadas de neuroimagen utilizadas en este estudio, lo que limita su utilidad en instalaciones más rurales y comunitarias. Por último, la aplicación general de este estudio puede verse aún más limitada por la población muy seleccionada de pacientes con AIS. Estos pacientes con AIS deben tener un infarto central pequeño y una penumbra isquémica más grande para obtener un beneficio potencial, mientras que el riesgo de hemorragia intracerebral sigue siendo el mismo que en estudios anteriores (es decir, 5-6%).
Conclusión clínica:
- Ya no deberíamos utilizar el paradigma "El tiempo es cerebro" en AIS. El avance de las neuroimágenes y las imágenes basadas en perfusión en una ventana extendida del accidente cerebrovascular es el futuro de la atención del accidente cerebrovascular al ayudar a identificar una población limitada de pacientes que se beneficiarían de la alteplasa sistémica frente a aquellos que no tienen ninguna posibilidad de beneficiarse en absoluto. La difícil decisión de administrar alteplasa sistémica debe basarse en el cuadro clínico general de cada paciente y debe venir después de una discusión profunda y compartida con el paciente y/o su familia, estableciendo explícitamente los beneficios y riesgos, incluidos los de muerte. y más hemorragia.
REFERENCIAS:
- Campbell BCV, et al. Ampliar la trombólisis a 4,5-9 h y despertar el accidente cerebrovascular mediante imágenes de perfusión: una revisión sistemática y un metanálisis de datos de pacientes individuales. Lanceta. 2019. PMID: 31128925
- Thomalla G, et al. Trombólisis guiada por resonancia magnética para el accidente cerebrovascular con tiempo de aparición desconocido. N Engl J Med 2018; PMID: 29766770
- Baliyan V, et al. Imágenes ponderadas por difusión: técnica y aplicaciones. Mundo J Radiol. 2016; PMID: 27721941
- Bakshi R, et al. La resonancia magnética con recuperación de inversión atenuada por líquido detecta lesiones de esclerosis múltiple corticales y yuxtacorticales. Arco. Neurol. 2001; PMID: 11346369
- Chen F, Ni YC. Desajuste difusión-perfusión de resonancia magnética en el accidente cerebrovascular isquémico agudo: una actualización. Mundo J Radiol. 2012; PMID: 22468186
- Emberson J, et al. Efecto del retraso del tratamiento, la edad y la gravedad del accidente cerebrovascular sobre los efectos de la trombólisis intravenosa con alteplasa para el accidente cerebrovascular isquémico agudo: un metanálisis de datos de pacientes individuales de ensayos aleatorios. Lanceta 2014; PMID: 25106063
- Nogueira RG, et al. Trombectomía de 6 a 24 horas después del ictus con desajuste entre déficit e infarto. N Engl J Med 2018; PMID: 29129157
- Albers GW, et al. Trombectomía por ictus de 6 a 16 horas con selección por imagen de perfusión. N Engl J Med 2018; PMID: 29364767
Publicación revisada por pares por: Salim R. Rezaie, MD (Twitter: @srrezaie )
La publicación Ampliación de la trombólisis sistémica a 4,5 – 9 horas y accidentes cerebrovasculares al despertar mediante imágenes de perfusión: un metaanálisis apareció por primera vez en REBEL EM - Blog de medicina de emergencia .
